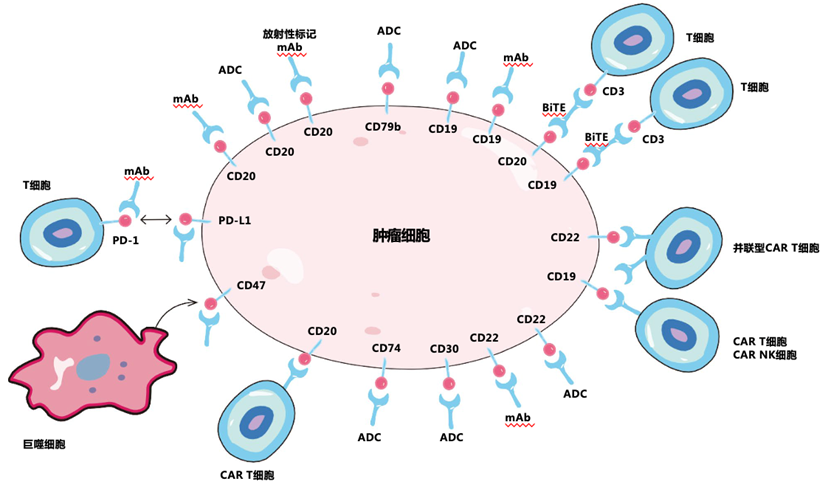
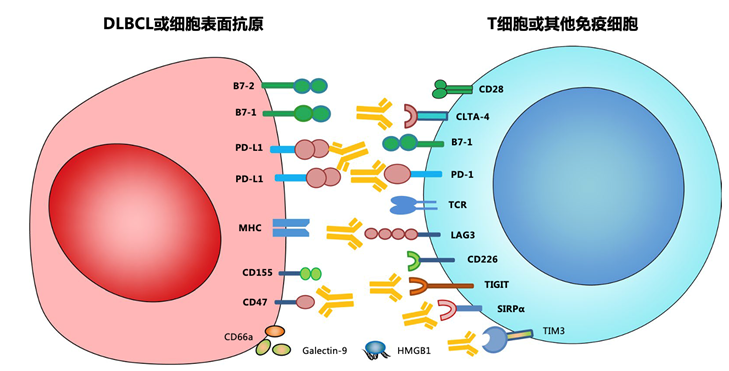
纵观国内外弥漫大B细胞淋巴瘤的治疗模式, R-CHOP(利妥昔单抗联合环磷酰胺、多柔比星、长春新碱、强的松)方案是DLBCL患者一线治疗的首要选择。但鉴于DLBCL具有异质性强这一特性,仍有近1/3的患者因对R-CHOP方案产生耐药而出现难治性或复发性疾病。为此,研究人员开始尝试在R-CHOP方案的基础上添加新型靶向药物,即R-CHOP+X模式,但临床试验结果不尽人意,这些全新的药物组合模式并不能为DLBCL患者带来明显获益。在此背景下,研究人员开始了不断求索之路,旨在发现DLBCL的全新治疗方法。近年来,针对免疫检查点、肿瘤微环境、分子信号通路和表观遗传畸变的疗法以及细胞免疫疗法共同构筑了DLBCL药物研发的新局面。本文将围绕免疫治疗、单克隆抗体(mAb)和抗体药物偶联物(ADC)、分子通路抑制剂和表观遗传修饰药物进行简要概述。面对日新月异的医学发展,血液肿瘤治疗步入精准靶向和免疫治疗新时代。其中,嵌合抗原受体(CAR)-T细胞是一类极具发展前景的细胞免疫疗法,通过对T细胞进行基因修饰使其表现特异性抗体CAR,靶向结合特定抗原后激活细胞毒性T淋巴细胞,释放颗粒酶、穿孔素及多种细胞因子,导致肿瘤破坏。目前,已有两种抗CD19 CAR-T产品(axicabtagene ciloleucel和tisagenlecleucel)获得FDA批准上市。不过,虽然在疗效层面CAR-T展现了出色的治疗效果,但仍有近半数患者发生了3级以上的严重不良事件,主要包括细胞因子释放综合征(CRS)和神经毒性。因而,如何在保持疗效的同时进行毒性管理是目前亟待解决的问题。目前,围绕有效性和安全性CAR-T的开发已初具成效,主要有并联型CAR-T(同时靶向CD19和CD20/CD22)和带有安全开关的CAR-T。另外,CAR-NK细胞有望成为CAR-T细胞的替代疗法,但仍需更多的试验进行验证。总的来说,不同靶点、不同组合或不同来源的多种CAR-T或NK细胞产品正不断丰富治疗DLBCL的武器库。双特异性T细胞衔接器(BiTE)是另一类全新的免疫治疗,能够与细胞毒性T细胞表面分子标志物CD3和肿瘤相关抗原(CD19/CD20)相结合,能够以MHC非依赖性方式诱导多克隆T细胞定向裂解肿瘤细胞。目前,已有多项关于BiTE治疗R/R DLBCL的临床试验正在开展之中,主要产品包含抗CD3-CD19 (Blinatumomab)和抗CD3-CD20 (Glofitamab、mosunetuzumab 和 REGN1979)的BiTE。图1. 针对 DLBCL 细胞表面抗原的新型药物和治疗方式除此之外,免疫调节剂和免疫检查点抑制剂也是免疫治疗的重要组成部分。来那度胺是一种比较常见的免疫调节剂,能够围绕免疫系统发挥多重作用,并且还通过影响参与维持肿瘤生长和存活的细胞因子的产生和活性来改变肿瘤微环境。同时,来那度胺还可通过与cereblon结合,抑制下游NF-κB信号传导,发挥直接的肿瘤毒性作用。同时,在R/R DLBCL的临床试验中,围绕来那度胺的联合治疗方案(诸如R2、R2-CHOP、R-ICE等)表现出良好的临床效益。鉴于免疫逃避是DLBCL的重要标志之一,对于免疫检查点抑制剂的开发不可或缺。除常见的PD-1和PD-L1外,目前已有多种新型的免疫检查点抑制剂(LAG-3、TIGIT、TIM3和VISTA)的靶标不断被发现,但仍有待在DLBCL中进行验证。图2. DLBCL中的免疫检查点靶标和相应的免疫检查点抑制剂由于利妥昔单抗在DLBCL治疗中的突出表现,围绕肿瘤细胞表面抗原的mab和ADC药物的研发,一直以来都是科研重心。目前,临床研发的三大类单克隆抗体,主要包含抗CD20 mAb、抗CD19 mAb和抗CD22mAb。为了更精准地杀伤肿瘤细胞,被称为“生物导弹”的ADC药物应运而生。ADC由单克隆抗体、偶联链和细胞毒性小分子三部分组成,主要通过单克隆抗体与肿瘤细胞表面的特异性抗原结合,利用抗原与抗体的特异性,将细胞毒药物定向递送到肿瘤病灶,具有超强的靶向肿瘤杀伤效果和能力。现今,已有相关研究初步验证了,ADC药物在DLBCL治疗中的作用。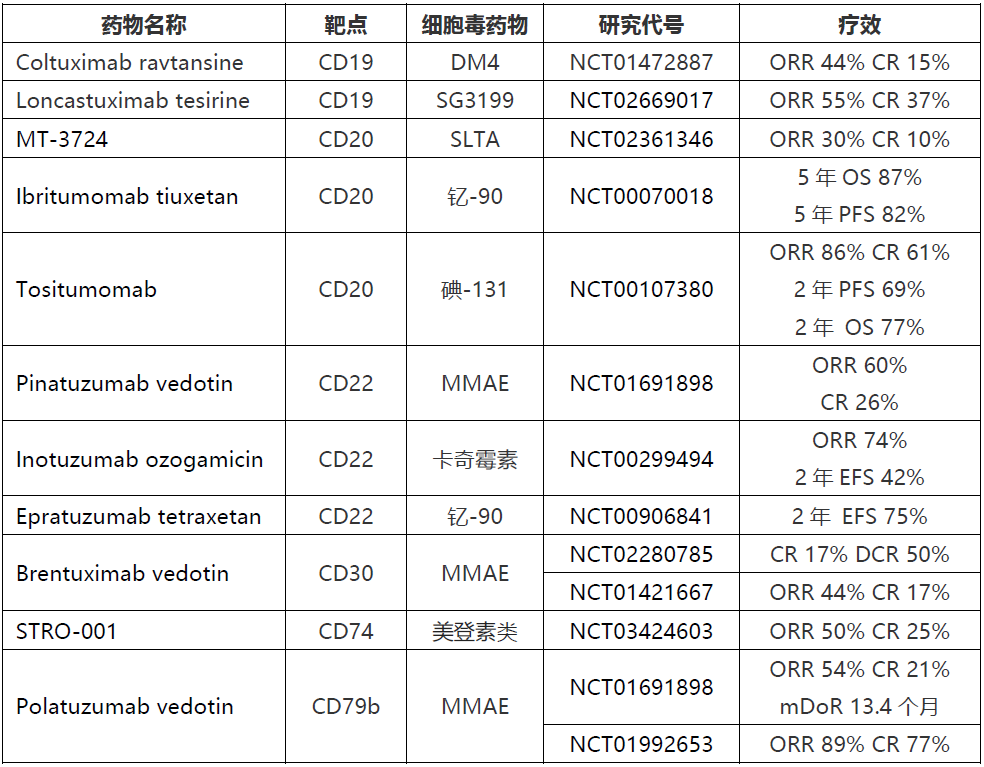
MMAE,一甲基澳瑞他汀E;SLTA,志贺毒素A1;mDoR,中位缓解持续时间;EFS,无事件生存率;ORR,客观缓解率;CR,完全缓解;OS,总生存率
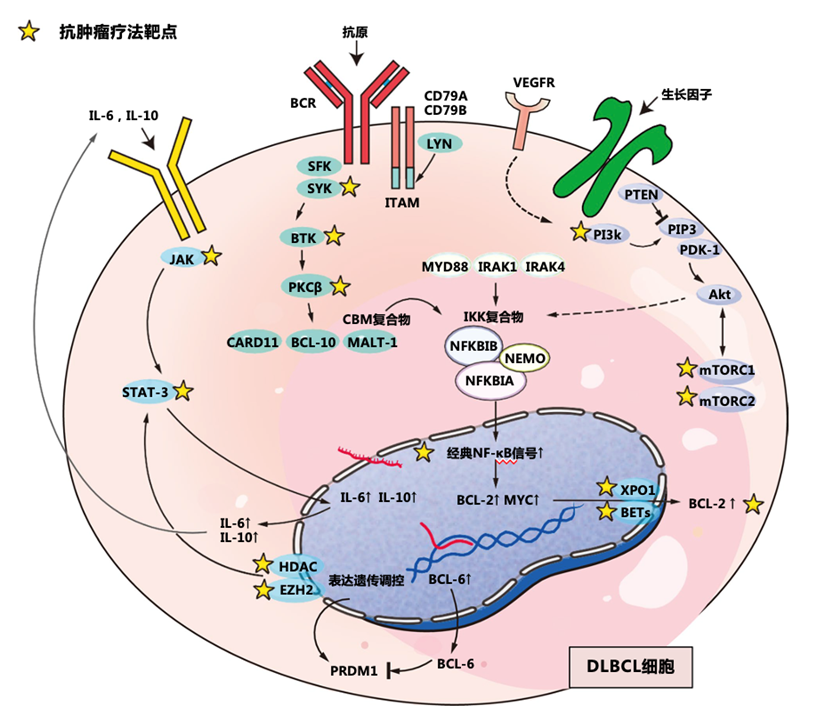
随着高通量测序平台的应用,DLBCL发生发展涉及的异常基因和分子信号通路逐步被阐明,主要涉及B细胞受体(BCR)信号通路、NF-κB信号通路、JAK/STAT3信号通路、PI3K/AKT/mTOR信号通路、BCL-2家族功能异常、组蛋白修饰异常等。目前,已有许多针对DLBCL发病相关异常基因及信号通路研发的靶向药物已进入临床或正处于研发试验阶段,如布鲁顿酪氨酸激酶(BTK)抑制剂、蛋白酶体抑制剂、mTORC1抑制剂、组蛋白甲基转移酶(EZH2)抑制剂等等。编者认为虽然目前DLBCL药物研发管线呈现出“百家争鸣”的格局,各类联合治疗模式层出不穷,但是由于患者资源有限,因而导致临床试验开展难度增加。因此,未来应尽可能探索可靠的生物标志物来指导个体化治疗,筛选具有潜在减毒增效联合治疗方案,来指导临床试验的开展。最后,虽然DLBCL的治愈之路任重而道远,但当深入了解DBLCL遗传学信息后,必将会出现新药与传统药物的最佳组合,推动DLBCL的精准治疗的发展。
1.Raut LS, et al. Management ofrelapsed-refractory diffuse large B cell lymphoma. South Asian J Cancer. 2014Jan;3(1):66-70.
2. Wang L, et al. New agents and regimensfor diffuse large B cell lymphoma. J Hematol Oncol. 2020 Dec 14;13(1):175.
3. 曾静, 等. 复发难治弥漫大B细胞淋巴瘤治疗进展. 白血病·淋巴瘤,2020,29(12): 757-761.
4. Clémentine Sarkozy, et al. New drugs for themanagement of relapsed or refractory diffuse large B-cell lymphoma. Annals ofLymphoma.2019;3:10.
如需要文献全文,请在下方留言并提供您的邮箱