 歆语健康发布于 3周前
歆语健康发布于 3周前 收藏专家
收藏专家原发性中枢神经系统淋巴瘤(PCNSL)是一种罕见但极具侵袭性的非霍奇金淋巴瘤,局限于脑、脊髓、软脑膜或眼内,超过90%为弥漫大B细胞型。尽管近年来诊疗技术不断进步,其5年生存率仍仅为29.9%,且约35%-60%患者在两年内复发,预后极差。传统以大剂量甲氨蝶呤为基础的化疗联合放疗虽有一定疗效,但毒性显著,尤其对老年及体弱患者耐受性差,亟需更安全有效的替代方案。
随着基因组学、转录组学和单细胞测序技术的发展,PCNSL的分子发病机制逐渐清晰:NF-κB通路异常激活、MYD88/CD79B高频突变、免疫抑制性微环境形成等成为关键靶点。这些发现推动了靶向治疗与免疫疗法的迅猛发展。多项临床研究显示,BTK抑制剂、免疫调节剂、PD-1抗体乃至CAR-T细胞治疗在R/R PCNSL中展现出令人鼓舞的疗效。本文基于发表于《Frontiers in Immunology》的权威综述1,系统梳理当前PCNSL治疗领域的突破性进展与现实挑战,为临床决策提供前沿依据。
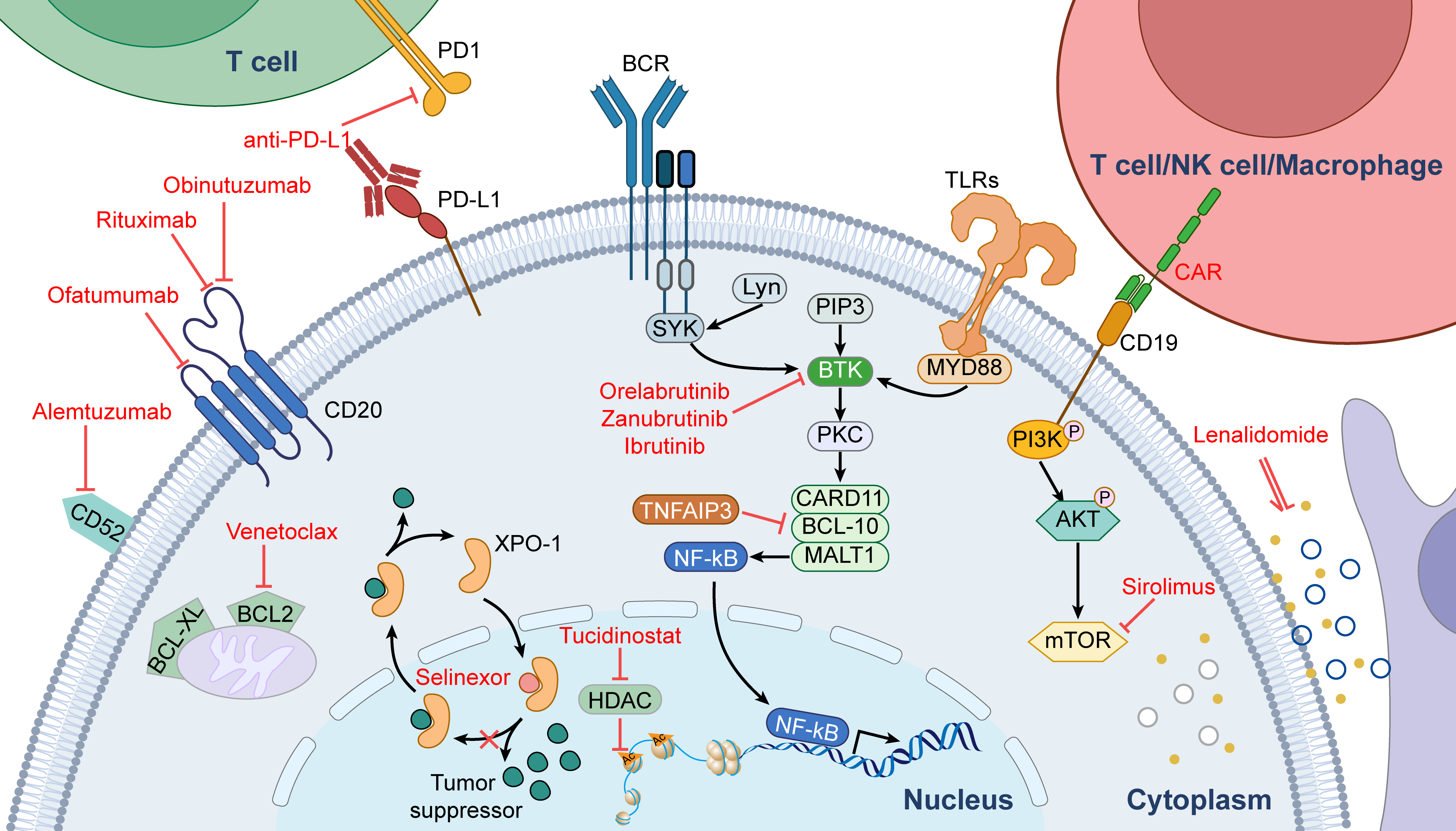
BTK(Bruton酪氨酸激酶)作为B细胞受体(BCR)信号通路的关键节点,在PCNSL的发生发展中起核心作用,尤其是携带CD79B和/或MYD88 L265P突变的患者,其肿瘤细胞对BCR信号高度依赖,因而成为理想靶点。第一代BTK抑制剂依鲁替尼因其可快速穿透血脑屏障(约0.29小时达中枢病灶),并在脑组织中达到较高浓度而备受关注。
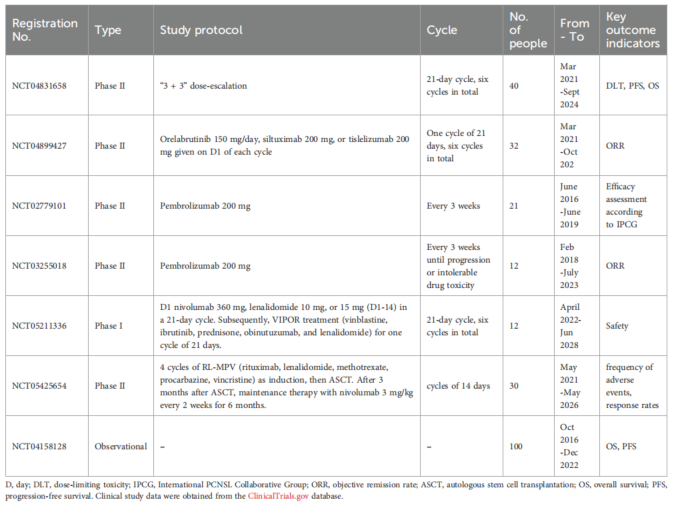
一项Ib期研究纳入18例初诊或复发/难治性PCNSL患者,使用依鲁替尼单药治疗后,94%患者肿瘤体积缩小;在后续联合利妥昔单抗、替莫唑胺等方案中,可评估患者的完全缓解率达86%。另一项剂量递增研究显示,依鲁替尼联合大剂量甲氨蝶呤和利妥昔单抗用于复发/难治性PCNSL,客观缓解率高达77%,中位无进展生存期4.6个月,且安全性可控。值得注意的是,该疗效优于系统性复发/难治DLBCL(25%),提示PCNSL可能对BTK抑制剂更具敏感性。
免疫微环境重塑:
来那度胺与PD-1抑制剂双线并进
PCNSL具有典型的免疫逃逸特征,肿瘤微环境中存在大量表达PD-1的T细胞浸润淋巴细胞(TILs)和表达PD-L1的肿瘤相关巨噬细胞(TAMs),形成高度免疫抑制状态,高PD-1表达与较差总生存相关。这一机制为免疫调节剂和免疫检查点抑制剂的应用提供了理论基础。
来那度胺作为第二代免疫调节药物,可通过刺激T细胞和NK细胞扩增、抑制NF-κB通路及拮抗IRF4/MYC促生存信号发挥多重抗肿瘤效应。法国多中心II期研究显示,来那度胺联合静脉利妥昔单抗治疗复发/难治性PCNSL(含眼内淋巴瘤),缓解率达70%,中位无进展生存约8个月,总生存约19个月。另有小样本研究提示,来那度胺作为挽救治疗后的维持方案,可使部分患者维持完全缓解超过2年,展现其巩固治疗潜力。
细胞免疫治疗曙光初现:
CAR-T疗法的安全性与持久性探索
CAR-T细胞疗法作为血液系统肿瘤领域的革命性手段,正逐步拓展至PCNSL领域。尽管早期因担心细胞因子释放综合征(CRS)、CAR-T相关脑病综合征(CRES)和神经毒性而被排除在多数试验之外,但随着技术优化,越来越多研究开始纳入CNS受累患者。
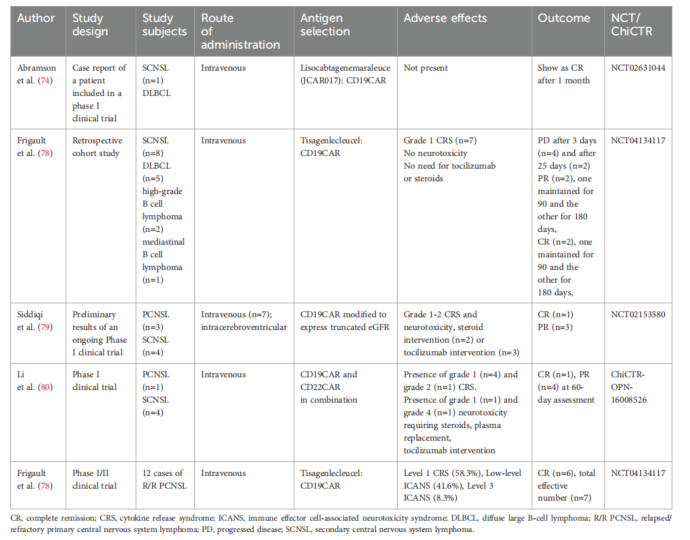
目前已有多项临床研究报道CD19-CAR-T在PCNSL/SCNSL(继发性中枢神经系统淋巴瘤)中的应用。一项临床试验报告1例SCNSL患者在接受CAR-T治疗后,脑部病灶消退并维持完全缓解达12个月,且未发生CRS或CRES。一项纳入8例SCNSL的回顾性队列研究显示,CAR-T治疗后2例达完全缓解,2例部分缓解,仅轻微神经毒性,无需药物干预。一项I/II期试验显示,CRA-T治疗在12例R/R PCNSL中总体有效率为58.3%,完全缓解率达50%,3例持续完全缓解且无危及生命事件。
拓展阅读
液体活检技术正在为PCNSL的精准管理开辟新路径。PCNSL作为罕见且侵袭性强的非霍奇金淋巴瘤,传统诊断高度依赖立体定向脑活检这一有创手段,尽管其诊断准确率达73%-97%,却存在血肿、癫痫等并发症风险(约1%患者出现活检相关死亡),且诊断流程耗时易导致治疗延迟;而常规无创手段如脑脊液(CSF)细胞学、流式细胞术敏感性极低(分别仅13.3%、23.3%),难以满足临床需求。
液体活检通过分析体液中肿瘤衍生标志物,为PCNSL提供了无创、精准的诊断路径。其一,针对CSF中循环肿瘤DNA(ctDNA)的检测,尤其是MYD88突变(PCNSL中检出率58%-86%,以L265P突变为主),与IL-10联合检测时可将诊断敏感性提升至94%、特异性达98%;其二,CSF中特定microRNA(如miR-21、miR-19b、miR-92a组合)的诊断准确性优异(敏感性95.7%、特异性96.7%),且能动态反映PCNSL治疗响应与疾病状态,助力治疗监测;此外,液体活检还可克服传统组织活检的局限性,通过获取多部位肿瘤衍生的“循环”核酸,全面呈现肿瘤异质性下的分子特征,避免单一组织取样的代表性不足问题2。尽管液体活检相关检测仍需标准化验证,但已成为突破PCNSL诊断困境、推动其向无创化、精准化诊疗发展的关键技术方向。
PCNSL的治疗正经历从“化疗主导”向“靶向+免疫”范式的深刻转变。BTK抑制剂(如依鲁替尼、奥布替尼)凭借良好的中枢渗透性和显著疗效,已被NCCN指南推荐用于复发/难治性患者;来那度胺和PD-1抑制剂则通过重塑免疫微环境,展现出高缓解率和良好耐受性;CAR-T疗法虽处探索阶段,但初步数据显示其在控制中枢病灶方面的可行性与安全性正在提升。
参考文献
1.Yang C, et al.Front Immunol. 2025;16:1438001. Published 2025 Feb 18.
2.Baraniskin A, et al.Cancers (Basel). 2021;13(11):2665. Published 2021 May 28.










