 歆语健康发布于 1周前
歆语健康发布于 1周前 收藏专家
收藏专家原发性免疫性血小板减少症(ITP)的经典病理机制,是自身抗体(AAb)介导的、依赖Fcγ受体(FcγR)的脾脏巨噬细胞对血小板的吞噬破坏。然而,越来越多的证据指向另一条“隐秘通道”——抗体诱导的血小板去唾液酸化及其介导的Fc非依赖性肝清除。传统观点认为,抗血小板糖蛋白GPIbIX抗体更易诱发去唾液酸化。但这一认知正被挑战。最新来自维也纳的队列研究,带来了颠覆性的发现:在近三成成人原发性ITP患者中检测到显著的血清诱导血小板去唾液酸化能力,且这种能力竟与抗GPIIbIIIa抗体的存在显著相关,而非原先认为的GPIbIX!更令人意外的是,这种“脱糖”现象虽然与更严重的临床出血表型挂钩,却与患者血小板计数高低、疾病分期(新诊断vs慢性)、治疗需求甚至脾切除状态没有关联。
与既往认知不同,去唾液酸化能力与抗GPIIbIIIa抗体的存在显著正相关(p=0.020)。在38例有去唾液化能力的患者中,50% (19/38) 检测到血小板结合AAb,其中高达39.5% (15/38) 是抗GPIIbIIIa抗体。而在无去唾液化能力的95例患者中,仅28.4% (27/95) 有AAb,其中仅20.0% (19/95) 是抗GPIIbIIIa抗体。抗GPIbIX或双阳性抗体与去唾液化能力的关联无统计学差异。

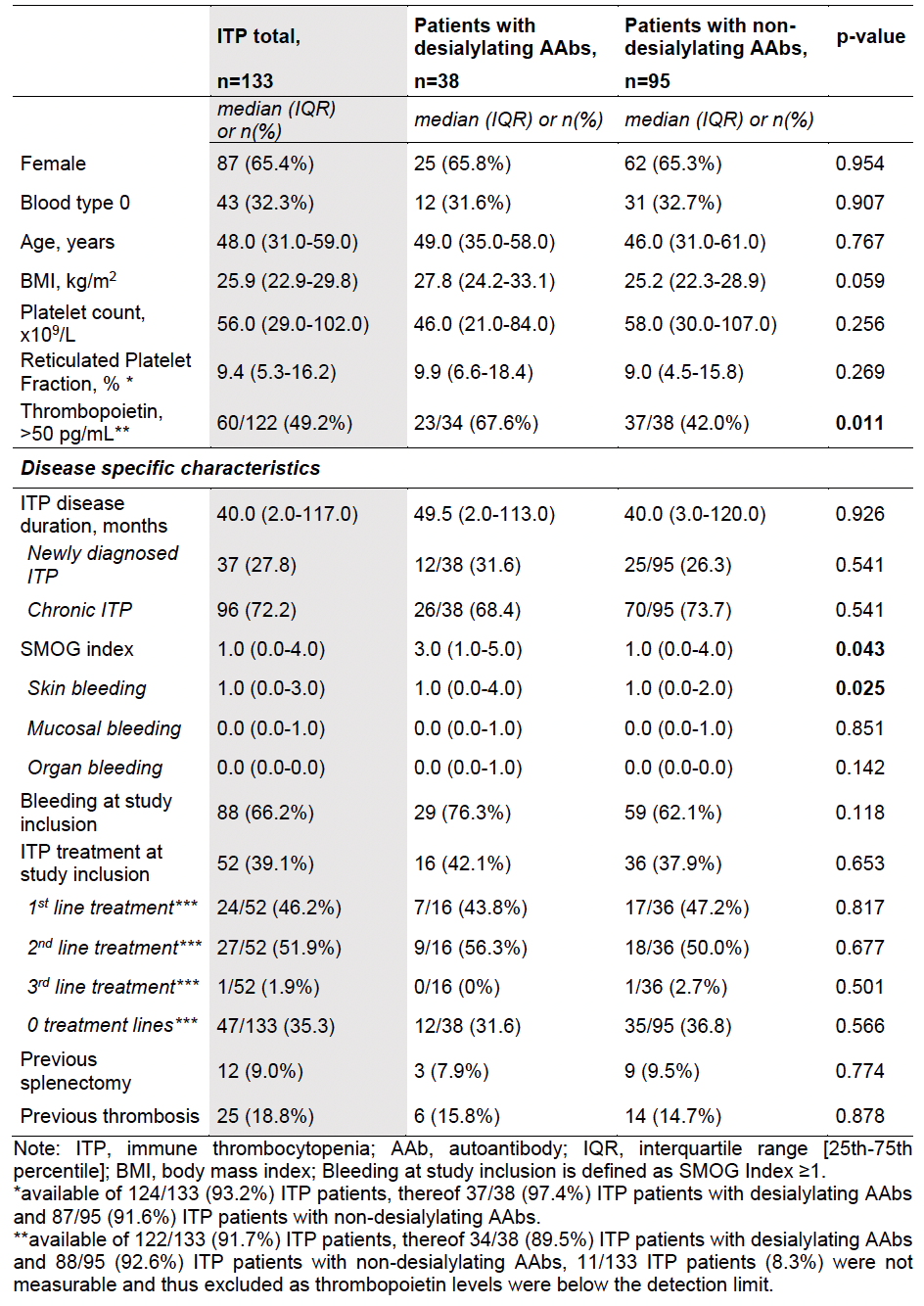
表2. 依据血小板是否去唾液酸化分层患者的临床特征
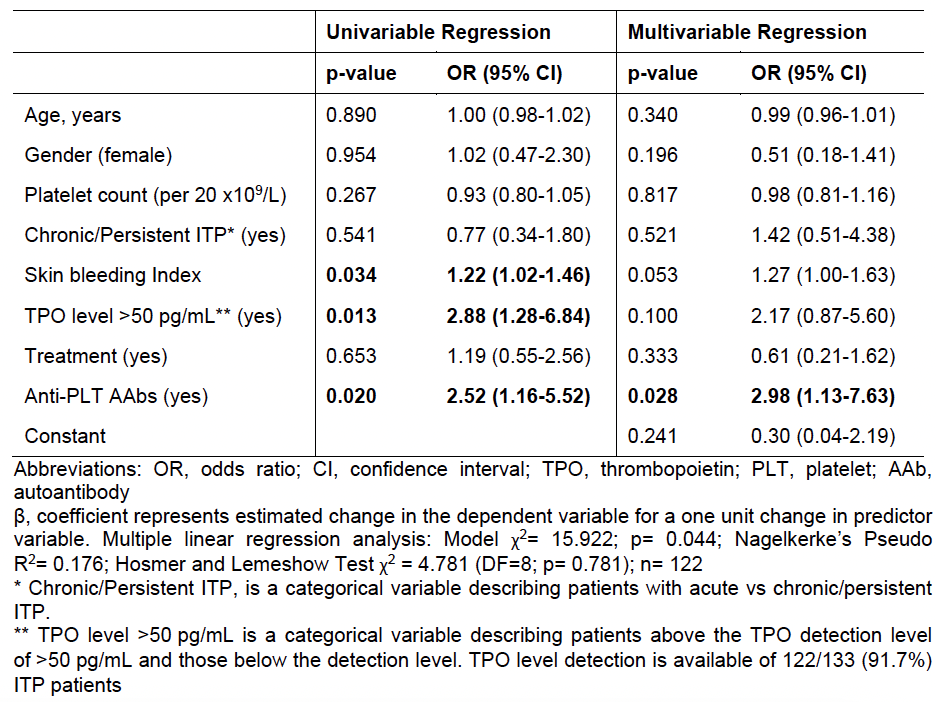
表3. 关于血小板去唾液酸化的多因素分析
拓展阅读
血小板去唾液酸化:从分子机制到治疗曙光
血小板表面覆盖着富含唾液酸的糖萼。唾液酸作为末端糖基,对维持血小板寿命和功能至关重要。当自身抗体(特别是通过其Fab片段)结合血小板糖蛋白(如GPIIbIIIa或GPIbIX)时,可触发细胞内神经氨酸酶(如Neu1, Neu3)转位至细胞膜,催化水解唾液酸,导致去唾液酸化2-3。
暴露的次末端糖基(主要是β-半乳糖)被肝细胞表面的Ashwell-Morell受体(AMR)识别。这种识别不依赖于抗体的Fc段,因此绕过了经典的脾脏FcγR依赖的清除途径,直接将血小板导向肝脏清除。这就是Fc非依赖性血小板清除的核心机制2-4。
有趣的是,AMR识别去唾液化血小板后,不仅介导清除,还会通过JAK2-STAT3信号通路上调血小板生成素(TPO) 的合成,形成一种代偿性反馈回路,试图抵消血小板减少。
维也纳研究重塑了ITP病理认知框架:首先,证实抗GPIIbIIIa抗体是血小板去唾液化的主要驱动者,颠覆了既往"GPIbIX中心论";其次,揭示去唾液化通过损害血小板功能(尤其GPIIbIIIa受体活性)而非仅加速清除导致出血,解释了为何其与血小板计数无关却显著加重临床出血;最后,证明这是独立于疾病分期和治疗状态的稳定病理特征。研究局限在于检测方法学(SASPA法可能低估GPIbIX抗体)和单一时间点观察。未来需深入探索:①抗GPIIbIIIa抗体触发神经氨酸酶转位的分子开关;②去唾液化对血小板聚集/粘附功能的量化影响;③基于"抗体类型+脱糖程度"的分层治疗策略。随着靶向神经氨酸酶的新型抑制剂研发,ITP治疗或将进入"纠正血小板功能损伤"与"提升血小板数量"并重的新时代。
参考文献
1.Schramm T, et al. Clinical Evidence for Anti-GPIIbIIIa Antibody-Induced Platelet Desialylation in Primary Immune Thrombocytopenia. J Thromb Haemost. 2025 Jun 3:S1538-7836(25)00343-5.
2.Cines, D.B., J.B. Bussel, H.A. Liebman, and E.T. Luning Prak, The ITP syndrome: pathogenic and clinical diversity. Blood, 2009. 113(26): p. 6511-21.
3.Li, J., et al., Desialylation is a mechanism of Fc-independent platelet clearance and a therapeutic target in immune thrombocytopenia. Nat Commun, 2015. 6: p. 7737.
4.Wang, Y., et al., Desialylation of O-glycans on glycoprotein Ibalpha drives receptor signaling and platelet clearance. Haematologica, 2021. 106(1): p. 220-229.
5.Sun, L., et al., Dexamethasone plus oseltamivir versus dexamethasone in treatment-naïve primary immune thrombocytopenia: a multicentre, randomised, open-label, phase 2 trial. Lancet Haematol, 2021. 8(4): p. e289-e298.










