 歆语健康发布于 1周前
歆语健康发布于 1周前 收藏专家
收藏专家多发性骨髓瘤(MM)是一种以克隆性浆细胞异常增殖为特征的恶性血液系统肿瘤,其发病机制复杂,临床表现异质性显著,导致疾病管理面临巨大挑战。随着对MM分子生物学认识的深入和新型治疗技术的涌现,如何突破现有治疗瓶颈、实现更深层次且持久的疾病控制,成为血液肿瘤领域亟待解决的核心议题。

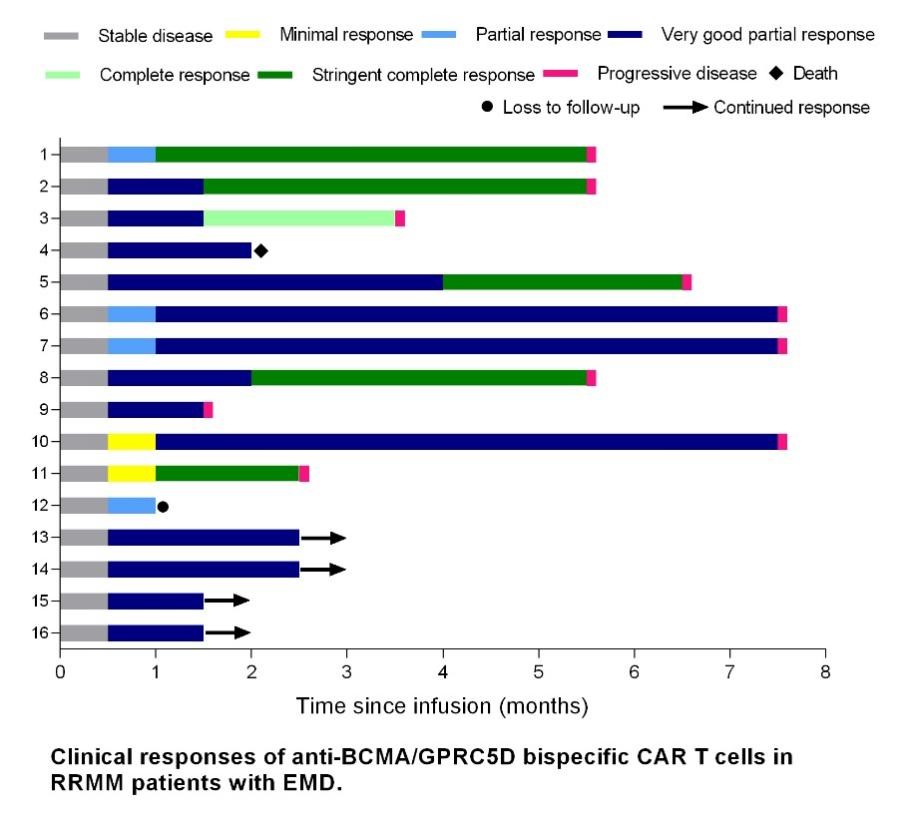
本次EHA年会上中国研究团队报告了一项重要成果(摘要PS2147),其研发的抗BCMA/GPRC5D双靶点CAR-T疗法在16例伴髓外病变的难治性骨髓瘤患者中取得100%客观缓解率。数据显示,38%患者达到完全缓解,94%实现微小残留病阴性,中位起效时间仅30天。
拓展阅读
一线CAR-T疗法在高危新诊断多发性骨髓瘤中展现持久缓解
尽管新诊断高危多发性骨髓瘤(HR-NDMM)患者接受移植治疗,但预后情况依然不容乐观。而一项针对22例适合移植的HR-NDMM患者的研究(摘要PS1711)带来了令人振奋的消息,其结果表明,GC012F/AZD0120双靶点CAR-T作为一线疗法展现出卓越疗效。具体来看,该疗法实现了100%的客观缓解率(ORR)和95.5%的严格完全缓解(sCR)率,尤为值得注意的是,所有患者均达到微小残留病(MRD)阴性(灵敏度10-6)。
在长期疗效方面,中位随访32.3个月时,30个月无进展生存率(PFS)达到85.7%,并且中位缓解持续时间(DOR)及PFS尚未达到,这意味着该疗法的有效性具有可持续性。不仅如此,在安全性层面,GC012F/AZD0120双靶点CAR-T疗法同样表现优异,仅27%的患者发生1-2级CRS,未出现≥3级CRS或免疫效应细胞相关神经毒性综合征(ICANS)。同时,CAR-T细胞峰值扩增显著(中位62,131拷贝/μgDNA),为治疗效果提供了有力支撑。
此外,该疗法采用FasT CAR-T快速生产平台,能够实现次日制造,极大缩短了治疗准备时间。其出色的长期缓解数据与良好的安全性,有力地挑战了传统“诱导-移植”模式,为HR-NDMM患者的治疗带来新的希望,有望成为此类患者的标准治疗方案。
序贯BCMA CAR-T疗法为RRMM患者带来新突破:真实世界研究证实100%缓解率与持久疗效
本次会议上公布的一项突破性研究(摘要PF758)显示,序贯使用两种不同的BCMA靶向CAR-T细胞产品(Ide-cel后接Cilta-cel)治疗复发/难治性多发性骨髓瘤(RRMM)患者,不仅展现出显著的临床效益和良好的安全性,还为CAR-T治疗后复发这一临床难题提供了创新解决方案。这项在德国三家CAR-T治疗中心开展的真实世界研究表明,在10例接受序贯治疗的患者中,第二次CAR-T(Cilta-cel)治疗的总体缓解率(ORR)达到100%,其中70%患者获得CR或更好,且12个月无进展生存(PFS)率为65%。
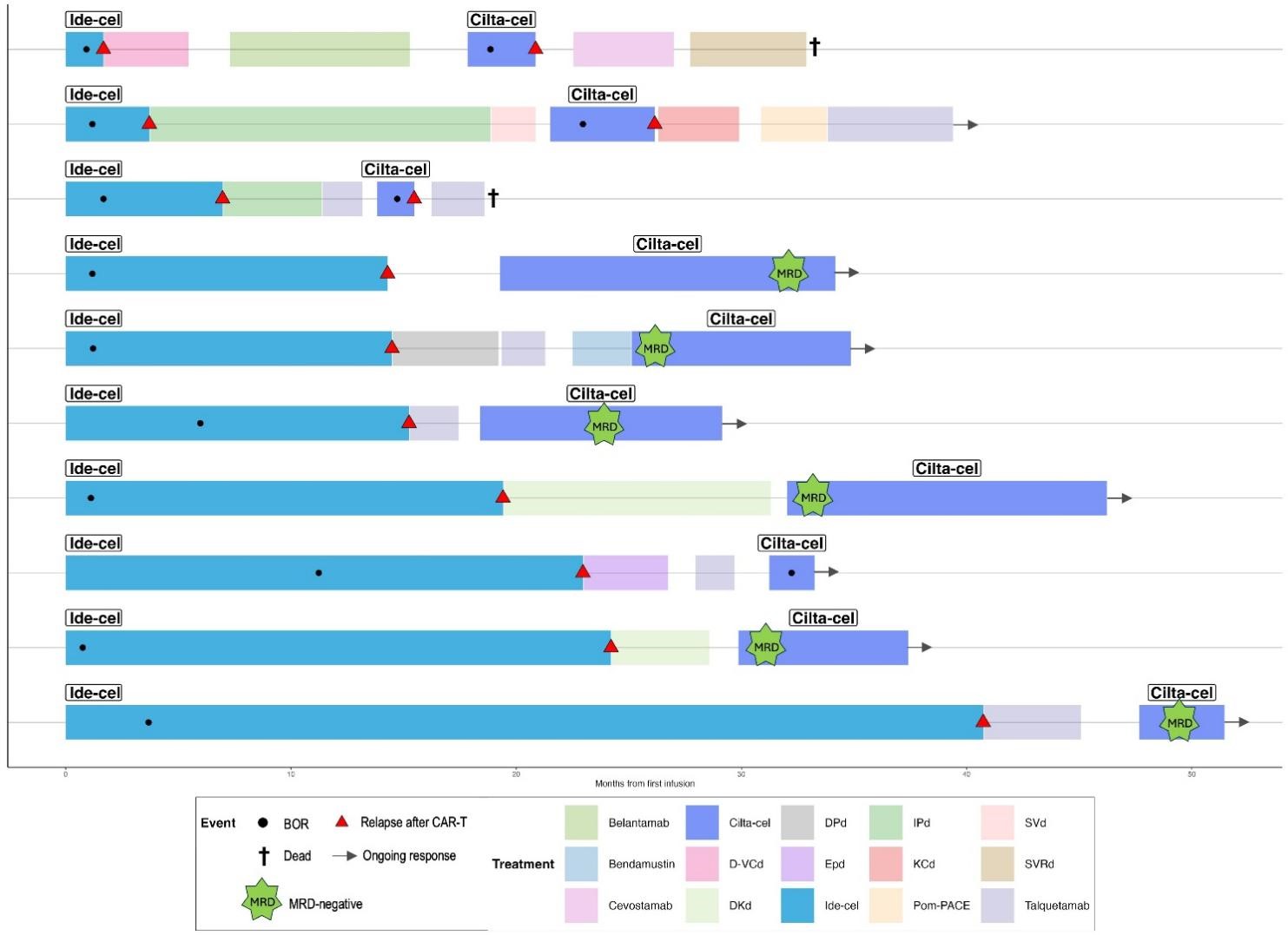
图2.不同患者接受CAR-T细胞疗法治疗的时间线和治疗结果
拓展阅读
Cilta-Cel治疗相关肠结肠炎的风险因素与管理策略
本次EHA年会即将公布一项突破性研究(摘要PS2119),该研究开发的新型单域抗体(sdAb)BCMA CAR-T细胞在临床前研究中展现出优于现有CAR-T产品的治疗效果。这项研究通过创新性地采用羊驼来源单域抗体作为识别元件,为改善MM免疫治疗效果提供了新思路。
研究团队从免疫羊驼的噬菌体展示库中筛选出多个BCMA特异性sdAb家族,并基于此构建了相应的第二代4-1BB共刺激结构域CAR-T细胞。相比现有ide-cel(scFv-CAR-T)和cilta-cel(双表位sdAb-CAR-T)疗法,新型sdAb-CAR-T细胞展现出显著优势。
具体来说,在细胞表型方面,新型sdAb-CAR-T细胞富含干细胞样记忆T细胞和中央记忆T细胞,且耗竭标志物(PD1、LAG-3、TIM-3)表达更低,这为其持久的免疫应答能力奠定基础;在抗肿瘤活性上,于MM小鼠模型实验中,sdAb5和sdAb10两种构建体的抗肿瘤效果显著优于ide-cel,其中sdAb5的疗效与cilta-cel相当,彰显出强大的抗癌潜力;在亲和力特征上,研究发现sdAb5单体的亲和力(KD值)与cilta-cel双表位构建体相当,很好地解释了两者相似的疗效表现。
然而,研究过程中意外发现,当将sdAb5和sdAb10组合成双表位CAR-T构建体时,由于KD值显著增加,导致CAR-T细胞与抗原解离受阻,反而降低了治疗效果。这一发现为今后双表位CAR-T的设计提供了重要指导。此外,sdAb5-CAR-T在保持与cilta-cel相当疗效的同时,可能具备更好的安全性特征,这些成果为开发新一代MMCAR-T疗法奠定了坚实基础。
综上所述,本次会议上公布的多项研究进展为MM治疗领域迎来了一系列的重大突破,同时也为这一预后不佳的疾病带来了新的曙光。中国团队研发的BCMA/GPRC5D双靶点CAR-T在髓外病变难治性骨髓瘤中实现100%客观缓解率,同时通过智能连接池技术优化了细胞制备流程,显著提升了生产效率。GC012F/AZD0120双靶点CAR-T采用连接池管理系统,确保了一线治疗中95.5%的严格完全缓解率和85.7%的30个月无进展生存率。基于连接池的序贯BCMA CAR-T治疗方案为复发患者带来100%再缓解率,而新型sdAb-CAR-T通过连接池技术优化,展现出更优的治疗潜力。这些技术突破与临床成果的结合,标志着多发性骨髓瘤治疗进入精准化、高效化的新时代。
参考文献:
1.https://library.ehaweb.org/eha/2025EHAAbstract:PS2147
2.https://library.ehaweb.org/eha/2025EHAAbstract: PB3029
3.https://library.ehaweb.org/eha/2025EHAAbstract: PS1711
4.https://library.ehaweb.org/eha/2025EHAAbstract: PF758
5.https://library.ehaweb.org/eha/2025EHAAbstract: PS2152










