导语
在全球范围内,结直肠癌(CRC)已成为第三大常见恶性肿瘤和第二大癌症死因。在我国,其发病率更是跃居第二位,仅次于肺癌。由于早期症状隐匿,约50%的患者确诊时已发生远处转移,导致预后极差,五年生存率不足15%1。随着精准医学的发展,KRAS、BRAF等分子标志物及微卫星不稳定性(MSI)状态对预后评估和治疗决策的指导价值日益凸显。其中,约10%的转移性结直肠癌(mCRC)患者存在BRAF突变,90%为恶性程度更高的V600E亚型——这类肿瘤常表现为低分化、黏液性特征,易转移至淋巴结和腹膜,且多见于老年女性,与MSI-H高度相关2。尽管靶向药物的引入为这类患者带来了生存获益,但临床实践中,肿瘤治疗相关血小板减少症(CTIT)发生率高达38%3,成为制约疗效的关键瓶颈。

病例概括
基本信息
患者女性,66岁
现病史:患者主诉因“便血3月余”于2024年3月就诊我院门诊,查体结果显示:下腹部轻压痛,无反跳痛及肌紧张,肝脾肋下未触及;肠镜及病理显示:直肠下端累及肛门见一环2/3周隆起溃疡性病变,病理符合直肠腺癌;基因检测显示:BRAF V600E突变,KRAS、NRAS野生型,MSS型,UGT1A1 6/6;直肠MR显示:直肠中下段癌,EMVI(+),MRF(+),伴直肠系膜筋膜内、直肠上动脉周围、双髂内多发淋巴结增大,双侧肛提肌粘连不除外;PET-CT结果显示:1、直肠远端管壁增厚,FDG代谢水平增高,符合恶性(直肠癌),注意阴道上段受累;2、双侧盆壁、髂血管走行区、腹膜后多发淋巴结FDG代谢增高,转移可能大;3、子宫FDG代谢水平增高,内膜癌可能大,建议宫腔镜检及病理检查;4、左下肺结节,FDG代谢增高,考虑转移;诊断性刮宫病理显示:(子宫内膜)结合病史及免疫组化,符合肠腺癌转移。
既往史:糖尿病5年余,否认高血压、冠心病、脑梗等。
个人史:否认吸烟、饮酒史。
家族史:无肿瘤家族史。
临床诊断
治疗过程
抗肿瘤治疗
2024年3月至5月行化疗联合靶向治疗,具体方案为“CAPEOX+贝伐珠单抗”4周期,疗效评价PR(部分缓解);
2024年6月至8月继续行化疗联合靶向治疗,具体方案为“FOLFIRINOX+贝伐珠单抗”4周期,2周期治疗后疗效评价PR,所有4周期治疗结束后疗效维持PR;
2024年9月行直肠癌根治术(miles术)+全子宫切除及双侧附件+阴道部分切除术,肺转移暂不处理,术后病理显示:1、(直肠)符合化疗后改变,未见癌组织残留,局灶见低级别上皮瘤变,肿瘤退缩分级:0(完全反应);2、肛门断端、直肠断端未见癌;3、肠系膜淋巴结N1、N2、N3反应性增生(0/4,0/4,0/2),左侧盆腔、右侧盆腔淋巴结反应性增生(0/2,0/5);4、阴道壁受侵处未见癌组织,见粘液湖;5、萎缩性宫内膜,慢性宫颈炎,子宫平滑肌瘤;6、双附件未见特殊;疗效评价pCR(病理学完全缓解);
支持治疗
患者经“CAPEOX+贝伐珠单抗”治疗后出现I度中性粒细胞减少和II度血小板减少,中性粒细胞计数(ANC)和血小板计数(PLT)分别为1.54×109/L和65×109/L,于2024年5月21日至27日给予重组人血小板生成素(rhTPO) 15000U+7500U qd 皮下注射共7天和重组人粒细胞刺激因子进行对症治疗,患者血小板计数于5月27日回升至108×109/L(图1)。
2024年6月至7月给予rhTPO和TPO受体激动剂进行二级预防,具体方案为:rhTPO 15000U d2-d6 皮下注射与海曲泊帕 5mg d2-d6 口服,治疗期间患者再次出现II度中性粒细胞减少症(ANC为1.2×109/L)和II度血小板减少(PLT为60×109/L),并且出现I度转氨酶升高(75U/L)和I度神经毒性,随后在7月至8月治疗期间分别进行了对症升白、保肝降酶和对症营养神经支持,相应不良反应均有所好转,但患者仍然出现了II~III度血小板减少(最低PLT为48×109/L)(图1)。
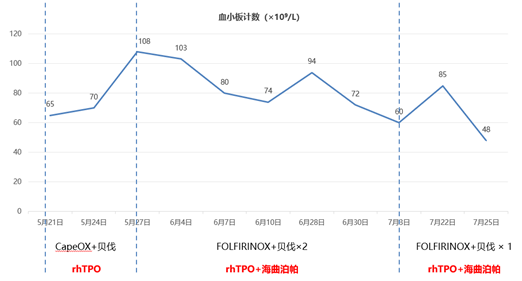
图1,患者血小板计数变化及用药方案
考虑到rhTPO联合海曲泊帕二级预防并未明显改善患者PLT,于2024年7月25日换用罗普司亭N01进行升板干预,具体方案为:罗普司亭N01 250-320ug 1次/周,患者PLT得到改善(图2)。
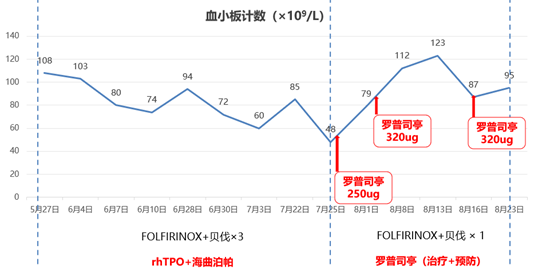
图2,患者血小板计数变化及用药方案
“FOLFIRINOX+贝伐珠单抗”治疗3周期后,患者PLT未得到有效改善,于7月25日换用罗普司亭N01进行升板干预,具体剂量为250μg,随后分别于8月1日和16日给予罗普司亭N01 320μg。
2024年11月至2025年3月维持治疗期间,给予罗普司亭N01 320μg 1次/周期 皮下注射进行预防性升板,化疗期间患者血小板维持在I度~正常范围内,并出现I度神经毒性。
治疗心得
本例患者确诊为IV期肠癌(cT4bN+M1)合并淋巴结转移、肺转移、子宫内膜转移。考虑到患者为初始潜在可切除的BRAFV600E突变型转移性直肠癌,虽然其预后较差,但仍有转化治疗机会,基于此,我们制定了以全身系统治疗为主的方案,旨在追求NED(无疾病状态)并延长生存期。在首次多学科团队(MDT)讨论后,我们选择采用“CAPEOX+贝伐珠单抗”方案进行4周期治疗,期间患者出现了严重血液学毒性,中性粒细胞计数(ANC)和血小板计数(PLT)分别为1.54×109/L和65×109/L,根据现行指南我们选择使用重组人血小板生成素(rhTPO)和重组人粒细胞刺激因子进行了对症治疗,患者PLT得到提升。
经第二次MDT讨论评估,患者对转化治疗反应良好,达到部分缓解(PR),整体耐受性也较好。为进一步提高治疗效果,我们尝试调整方案为“FOLFIRINOX+贝伐珠单抗”三药联合靶向治疗。同时考虑到患者在既往治疗中曾出现II度血小板减少(血小板计数最低≥50×109/L但<70×109/L)并且伴有出血的高风险因素,我们在三药治疗期间选择采用rhTPO+海曲泊帕进行二级预防,但患者在治疗期间血小板计数并未得到有效提升,PLT最低降至48×109/L。为进一步平衡高强度化疗带来的疗效与出血风险,我们选择在第三周期化疗后换用作用于天然位点的长效TPO-RA罗普司亭N01进行升板干预,患者接受每周一次250–320 μg剂量的罗普司亭N01治疗后,血小板水平明显改善,化疗顺利完成,肿瘤标志物亦得到明显下降。随后,于2024年9月为患者实施根直肠癌根治术(miles术)+全子宫切除及双侧附件+阴道部分切除术,术后病理学评估结果为pCR(完全缓解)。
术后,结合患者意愿,我们自2024年11月至2025年3月期间继续给予靶向联合化疗进行维持治疗,并在此阶段使用罗普司亭N01作为血小板减少的预防措施,整个维持治疗期间,患者未再出现严重血小板下降,血小板水平维持在I度~正常范围内。

专家点评
化疗相关性血小板减少症(CTIT)是肿瘤治疗中的常见并发症,可导致出血风险增加、治疗延迟或剂量降低,进而影响患者生存获益4。在BRAF V600E突变转移性直肠癌的治疗中,高强度化疗虽然能提高转化率,但同时CTIT风险也会明显增加,传统升板药物(如rhTPO、小分子TPO-RA)在疗效和安全性上存在一定局限5。罗普司亭N01作为第二代长效TPO受体激动剂,其独特机制(四肽结构结合TPO受体,激活STAT通路)可高效促进巨核细胞增殖分化,每周一次给药即能实现稳定升板,且不经肝脏代谢,肝肾安全性更优。上述病例中,患者在三药联合靶向治疗期间反复出现难治性CTIT,换用罗普司亭N01后血小板得以有效回升,最终顺利完成转化治疗并达到pCR,进一步展示了其在平衡晚期直肠癌疗效与安全性中的关键作用。

专家点评
转移性结直肠癌的诊疗需重视多学科团队(MDT)的全程管理6,尤其在BRAF突变等预后较差的患者中,治疗方案的动态调整还有助于平衡患者的转化潜力与治疗毒性。上述患者通过MDT讨论,先后尝试了CAPEOX联合贝伐珠单抗与FOLFIRINOX三药联合靶向治疗的方案,尽管转化治疗疗效显著,但期间CTIT一度成为制约疗效的关键因素。在MDT模式下,罗普司亭N01的引入充分体现了其在个体化升板防治中的优势。首先,罗普司亭N01的长效机制可覆盖高强度化疗的整个周期,预防性使用能有效提升患者PLT、减少治疗中断;此外,与海曲泊帕等小分子TPO-RA相比,罗普司亭N01不经肝脏代谢,对肝肾功能无明显影响,更适合高度密集治疗策略下的合并用药。未来临床实践中,对于高出血风险或既往升板失败的患者,或许可优先考虑使用罗普司亭N01进行干预,必要时还可尝试联用小分子TPO-RA以进一步提高升板效果。

专家点评
上述病例中,患者使用rhTPO联合海曲泊帕后血小板计数仍低于50×109/L,换用罗普司亭N01后才得以有效改善,进一步印证了罗普司亭N01的强效升板能力。从结构上来看,罗普司亭N01的卓越疗效可能主要源于两个方面:一方面,Fc恒定区延长半衰期,可实现每周一次给药;另一方面,Fc恒定区形成的4肽结构域,可结合巨核细胞表面的TPO受体,激活其内源性通路促进巨核细胞产生血小板,从而促进巨核细胞的增殖、分化、成熟,实现高效升板。此外,其独特的代谢途径,经FcRn回收而非肝肾代谢,还避免了肝酶升高和药物相互作用,在联合贝伐珠单抗等抗血管生成药物时更具安全性优势。随着循证医学证据积累,罗普司亭N01或将成为CTIT治疗的新标准,尤其适用于需强化治疗的BRAF突变直肠癌等高风险人群。

专家点评
BRAF V600E突变型直肠癌患者通常预后不良,传统治疗手段疗效有限。然而,近年来多项研究已证实,靶向治疗药物的引入显著改善了该类患者的预后与生存获益。在此基础上,BRAF靶向药物与免疫检查点抑制剂联合治疗的潜力也逐渐显现。例如,近期有一项II期研究,纳入37例BRAF V600 E突变的CRC患者,患者接受了PD-1抑制剂萨特利珠单抗(PDR001)联合BRAF抑制剂达拉非尼和MEK抑制剂曲美替尼的三联方案。研究结果显示,PD-1联合BRAF/MEK抑制的三联疗法的确认客观缓解率(cORR)为25%,较既往BRAF/MEK双靶联合治疗的对照组(7%)提升三倍以上2。然而,此类多药联合方案往往伴随着较高的血液学毒性发生风险,尤其是严重血小板减少(CTIT),成为限制治疗持续性与患者依从性的关键因素。本例患者的成功转化经验提示,将新一代长效TPO受体激动剂罗普司亭N01纳入转化治疗策略,不仅可改善血小板水平、保障治疗连续性,也有望为高强度靶免联合方案的临床实施提供安全保障。
参考文献:
1.曾薇,等.中华全科医学,2025,23(01):31-35+147.
2.Chen S, et al. Cancer Biol Med. 2024;21(6):473-483.
3.Epstein R S, et al. Advances in therapy, 2020, 37: 3606-3618.
4.中国抗癌协会肿瘤临床化疗专业委员会, 等.中华医学杂志, 2023, 103(33): 2579-2590.
5.中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症诊疗指南 2024版.
6.中国临床肿瘤学会(CSCO)结直肠癌诊疗指南 2024版.












