2025年4月在《柳叶刀》上发布的最新病例报告显示,CD19 CAR-T细胞疗法成功治愈一例多重难治性ITP患者,为B细胞驱动的自身免疫疾病治疗开辟了全新路径。该患者在7年间接受多种治疗后均复发,在单次输注CD19 CAR-T细胞后,实现了长达4个月的无治疗缓解,且血小板恢复正常。研究证实了该疗法不仅疗效显著,且具备良好的安全性和持久的有效性,为众多ITP患者带来了新的治疗希望。
该病例报告了一名35岁男性难治性ITP患者的完整治疗历程及创新性治疗成果。患者于2016年确诊ITP(抗GPIIb/IIIa抗体阳性),初期对泼尼松龙及利妥昔单抗治疗(2016-2018)反应良好。2018年复发后转为罗普司亭维持治疗, 2021年失效后,相继尝试多种二线药物(包括TPO-RA类药物、SYK抑制剂、免疫抑制剂等)及脾切除术均未能获得持续缓解。至2024年初,患者病情急剧恶化,血小板计数持续低于10×109/L,需反复接受大剂量地塞米松和IVIG抢救治疗。
2024年4月,经多学科评估后,同年7月患者接受实验性CD19 CAR-T细胞疗法(KYV-101),显示出优异的安全性和有效性:预处理(氟达拉滨+环磷酰胺)后输注的CAR-T细胞(1×108,CD4/CD8=75%:25%),仅引发1级CRS(第8天发热),托珠单抗治疗后迅速控制。细胞动力学显示典型扩增模式(第14天时外周血中的CAR T细胞扩增达到峰值457个细胞/μL),伴随深度B细胞清除(至第84天开始重建)。
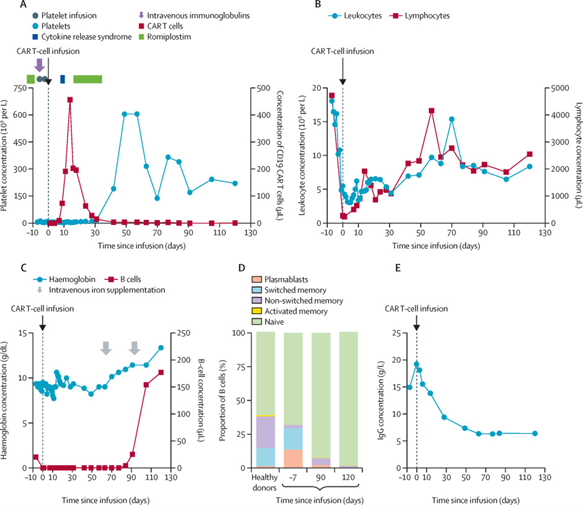
图1.:CD19 CAR-T细胞治疗原发性免疫性血小板减少症(ITP)患者的临床表现
(A)患者外周血中的血小板(正常范围150–375×109/L)和CAR-T细胞计数。(B)患者外周血中的白细胞(正常范围4–10×109/L)和淋巴细胞(正常范围1100–3020个/µL)浓度。(C)血红蛋白(正常范围13–18 g/dL)和B细胞(正常范围140–600个/µL)动态变化。(D)循环中CD21+ CD27–初始B细胞、转换(IgD–)和未转换(IgD+)CD27+ CD21–记忆B细胞、活化的CD20+ CD11c+ CD21–记忆B细胞以及CD38+ CD20–浆母细胞的组成,比较CAR-T细胞治疗前后与德国马格德堡输血医学研究所招募的15名健康供体的数据。(E)IgG浓度(正常范围7–16 g/L)。CAR=嵌合抗原受体。
本案例首次证实CD19 CAR-T疗法可诱导难治性ITP的持续免疫重建和临床缓解,其机制可能通过彻底清除自身反应性B细胞克隆实现。相较于传统治疗,该疗法展现出突破性的长期疗效,为难治性ITP提供了新的治疗选择,但远期疗效仍需更大样本和更长随访验证。
CD19 CAR-T细胞疗法为难治性ITP患者带来持久缓解与安全性保障
本病例展示了CD19 CAR-T细胞疗法在难治性免疫性血小板减少症(ITP)治疗中的突破性进展。该疗法通过深度清除自身反应性B细胞,成功实现了患者的长期临床缓解,为难治性ITP的治疗提供了全新的解决方案。治疗过程表现出良好的安全性特征,仅出现1级细胞因子释放综合征(CRS),且未发生严重的血细胞减少等不良反应。值得注意的是,患者的B细胞重建过程有序可控,第84天开始以初始B细胞为主进行重建。
拓展阅读
近年来,CAR-T疗法在癌症治疗中取得显著成效后,其应用范围逐渐扩展至自身免疫性疾病(AID)领域。传统AID治疗依赖免疫抑制剂或生物制剂,但部分患者疗效不佳或面临复发风险。CAR-T通过精准靶向致病性B细胞或自身反应性T细胞,为难治性AID提供了新思路。例如,在系统性红斑狼疮(SLE)和抗合成酶抗体综合征(ASS)中,靶向CD19或BCMA的CAR-T疗法已在小规模临床试验中展现出深度缓解甚至长期无药治疗缓解的潜力。2023年《自然·医学》报道的5例SLE患者经CAR-T治疗后均达到无药物缓解,且B细胞重建后未观察到复发,提示免疫系统“重置”的可能性。
观点评述
ITP治疗正面临重大变革——CD19 CAR-T疗法凭借深度清除自身反应性B细胞,使难治性ITP患者获得持久临床缓解,成功验证了“免疫系统重置”的治疗理念。这一突破不仅革新了ITP治疗模式,更为系统性红斑狼疮、抗合成酶抗体综合征等B细胞介导的自身免疫疾病提供了全新思路。
此外,我们仍需通过长期随访,深入探究B细胞重建后的免疫稳态维持机制,评估远期疗效与安全性。值得关注的是,全球多项II期临床试验(如KYV-101的KYSA-7研究)正在推进,将进一步明确CAR-T疗法在自身免疫病领域的应用价值。
随着临床研究的深入与治疗方案的优化,CAR-T技术有望成为难治性自身免疫疾病的关键治疗手段,推动治疗方向从症状控制迈向病因根治。未来,我们期待通过技术创新与临床转化,将这一疗法应用于更多自身免疫疾病,真正实现治疗领域的革命性突破。

参考文献
1.Trautmann-Grill K, et al.Lancet. 2025;405(10472):25-28.
2.Li M, Zhang et al.N Engl J Med. 2024;391(4):376-378.
3.Lambert MP, et al.Blood. 2017;129(21):2829-2835.
4.Yu TS, et al.Blood Adv. 2021;5(20):4087-4101.
5.Müller F, et al.N Engl J Med. 2024;390(8):687-700.












