以往的传统治疗手段难以从根本上扭转ITP病程,并且存在诸多局限性,难以从根本上改变疾病进程。而随着科研的不断深入,新型靶向治疗策略崭露头角,其中洛利昔珠单抗(Rozanolixizumab)——一种靶向FcRn的单抗,成为了ITP药物中的治疗新星。
2025年《BRITISH JOURNAL OF HAEMATOLOGY》上发布了两项洛利昔珠单抗治疗ITP的III期及开放标签扩展(OLE)结果。该药物通过抑制IgG回收,有效降低自身抗体水平,展现了快速升血小板能力,同时提出给药频率是疗效持续的关键因素,该研究为ITP的治疗带来了新方向。
TP0003(NCT04200456)和TP0006(NCT04224688)是两项平行开展的双盲、随机、安慰剂对照Ⅲ期临床研究,旨在评估洛利昔珠单抗治疗ITP的有效性与安全性。
研究聚焦于年龄≥18岁、确诊为持续性(病程3-12个月)或慢性(病程>12个月)的ITP患者,分别在北美、欧洲和亚洲的29个独立研究中心完成患者招募。入组标准严格限定患者基线血小板计数需低于30×109/L,且要求患者此前至少接受过一种ITP治疗。
研究采用2:1随机分组模式,借助交互式应答技术将患者分配至洛利昔珠单抗组或安慰剂组,并依据血小板计数(<或≥15×109/L)和脾切除史进行分层,确保组间基线特征均衡可比。
给药方案依据Ⅱ期研究结果制定,采用固定剂量策略:起始剂量约15mg/kg,随后每两周约10mg/kg维持。可根据血小板计数和不良事件调整剂量,如果降至约7mg/kg或280mg则固定剂量。该研究包括4周筛选期、24周治疗期及6周随访期,以合理评估药物长期效果。
疗效与安全性评估体系严谨且全面。主要研究终点设定为持久临床有意义的血小板反应(DCMPR),即要求患者在治疗第13-25周内,至少8/12次访视时血小板计数维持在≥50×109/L;次要终点则包括血小板≥50×109/L的累积周数、首次出现有效反应的时间等关键指标。安全性评估贯穿研究全程,密切监测治疗期间不良事件(TEAEs)、严重TEAEs以及特殊关注事件(如头痛、感染等)的发生情况,为药物安全性提供充分数据支撑。
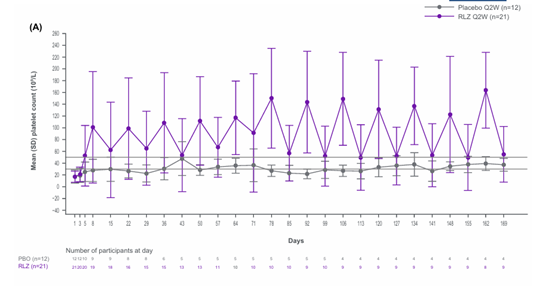
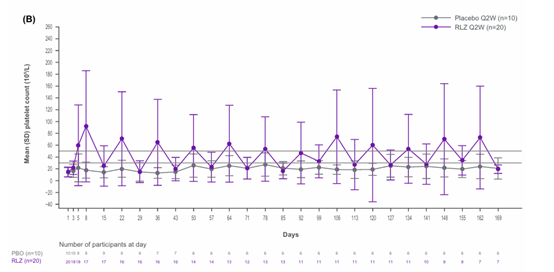
图2. TP0006 (双盲)随时间变化的平均血小板计数
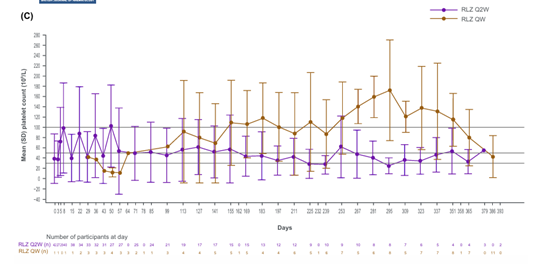
图3. TP0004(开放标签扩展)随时间变化的平均血小板计数
OLE作为后续补充,为完成双盲研究的患者提供了进一步治疗与观察的机会。患者可自愿进入TP0004(NCT04596995)为期1年的OLE研究,初始阶段采用每两周给药方案,后根据独立数据监查委员会的专业建议,调整为每周给药模式,重点评估长期治疗的安全性及血小板反应的持续性,为洛利昔珠单抗的临床应用提供更丰富的实践依据。
拓展阅读
开放标签扩展实验(OLE)是临床试验中的重要设计,通常在双盲对照试验完成后开展,旨在进一步评估药物的长期安全性、耐受性及有效性。与盲法试验不同,OLE阶段的研究者和受试者均知晓所用药物的真实性质,这种开放性设计有助于收集真实世界中的长期用药数据,尤其适用于慢性病或罕见病治疗方案的优化。
III期研究证实:
洛利昔珠单抗每周给药可快速持续提升ITP患者血小板计数,安全性良好
157例患者参与洛利昔珠单抗治疗ITP的研究筛查,最终63例患者被随机分组至TP0003(33例)和TP0006(30例)研究,其中43例进入OLE研究。患者基线特征较为平衡,且多数为慢性ITP患者,值得注意的是,TP0006组患者的中位病程(12.1年)显著长于TP0003组(5.2年)。
疗效方面,洛利昔珠单抗展现出显著优势。首次给药后第8天,TP0003和TP0006研究中,该药物治疗组分别有11/21和9/20的患者血小板计数≥50×109/L,而安慰剂组仅为2/12和1/10。
在持续反应上,TP0003组4/21、TP0006组1/20的患者达到持久临床有意义的血小板反应(DCMPR),安慰剂组则无患者达标;且在OLE研究中,每周给药能更有效地维持血小板计数≥50×109/L。从累积反应来看,洛利昔珠单抗组血小板≥50×109/L的累积周数明显高于安慰剂组(TP0003:7.6周vs.1.3周;TP0006:4.0周vs.1.4周)。
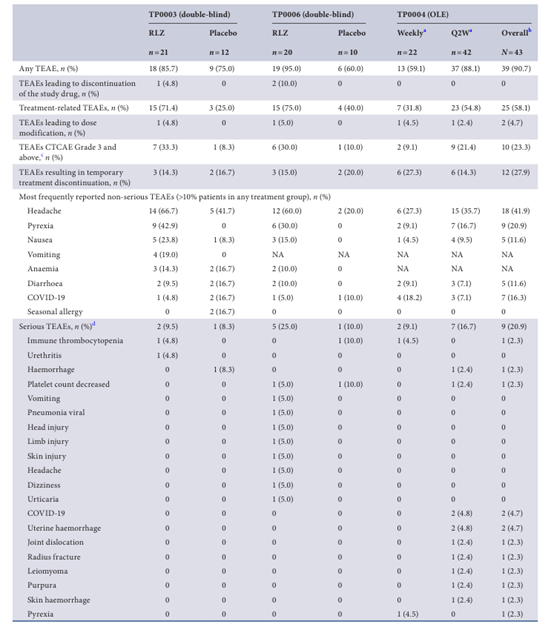
安全性上,治疗中出现的不良事件(TEAEs)大多为轻至中度,常见症状包括头痛、发热和恶心。严重TEAEs罕见,仅有5例被判定与治疗相关,涉及头痛、荨麻疹等症状。研究期间未出现死亡病例或机会性感染,即便IgG水平降低,也未增加患者感染风险。
药代动力学与免疫原性数据显示,洛利昔珠单抗血浆浓度在首次给药后3天达到峰值(约37.6-40.1μg/mL),后续维持剂量下浓度波动较大。其可使IgG水平快速下降,第8天便降至基线的54%-58%,每周给药则进一步增强IgG降低效果。尽管部分患者出现抗药抗体(ADA),但并未对治疗效果产生显著影响。
观点评述
作为ITP治疗领域的研究者,我们认为FcRn抑制剂虽为疾病治疗带来新突破,能快速提升血小板计数,但是它的疗效持久性受到给药频率和疾病异质性的制约。
基于当下的临床实践与研究进展,我们认为未来ITP治疗的突破需从多维度协同发力。在给药策略上,优化给药方案,开发长效制剂并探索个体化剂量;在联合治疗层面,与TPO-RA、SYK抑制剂等协同增效,实现机制互补。同时借助生物标志物实现精准治疗。此外,我们注意到,FcRn抑制剂在难治性ITP患者及老年、合并症人群中展现出独特优势,有望填补现有治疗空白。
随着不断科研技术的发展,对外泌体介导的补体激活、免疫代谢异常等发病机制的深入解析,我们坚信,未来的ITP治疗将更具针对性,通过个体化、精准化的综合策略,为不同亚群患者带来更优的治疗选择与预后改善。

参考文献
1.CooperN,et al.Br J Haematol. 2025;206(2):675-688.
2.Bril, V., et al.The Lancet. Neurology, 22(5), 383–394.
3.Singh A, et al.J Clin Med. 2021;10(4):789.
4.Smith B, et al.MAbs. 2018;10(7):1111–30.
5.Iraqi M, et al.Haematologica. 2015;100(5):623-632.












