再生障碍性贫血(AA)是一种以全血细胞减少和骨髓细胞减少为特征的血液系统疾病,可能导致慢性贫血、出血和感染。输血依赖性再生障碍性贫血(TD-NSAA)在整个AA患者人群中占比高,且并发症较多,单用环孢素治疗反应差,易进展为SAA,且目前关于探讨TD-NSAA最佳治疗方案的临床研究较少,临床医生对疾病认知尚不全面。血小板受体激动剂(TPO-RA)作为一种不具有免疫原性、口服给药的促血小板生成药物,在AA研究领域已被证实具有实现更高、更好血液学反应的能力,其在TD-NSAA患者中的治疗价值值得高度关注与深入探索。
NSAA不尽相同
输血依赖型患者长期生存显著恶化
AA并非罕见病,流行病学研究发现,在欧洲及北美地区,AA的发病率为2/100万,东亚地区高出欧美地区2~3倍1。目前,AA通常依据疾病严重程度分为3种类型 :重型再生障碍性贫血(SAA)、极重型再生障碍性贫血(VSAA)及非重型再生障碍性贫血(NSAA)。NSAA人群在总AA人群中占比高达80%,患者群体较为庞大,依据是否需要输注血制品进一步分为输血依赖型NSAA及非输血依赖型NSAA,但输血依赖型NSAA(TD-NSAA)目前尚无明确定义。在2022年推出的《再生障碍性贫血诊断与治疗中国指南》中,对TD-NSAA的定义为平均每8周至少1次成分输血且输血依赖持续时间≥4个月的患者,输血指征为血红蛋白≤60g/L;血小板计数(PLT)≤10×109/L,或PLT≤20×109/L伴有明显出血倾向2。一项在301例AA患者中开展的回顾性、长期随访研究显示,我国NSAA患者的整体预后较为良好,5年总生存率(OS)可达94.6%3。但是,TD-NSAA患者的5年OS显著低于NTD-NSAA患者(81.8% vs 98.8%,P<0.001)。这提示TD-NSAA患者面临着沉重的疾病负担,亟需临床重视和关注,给予更为积极的治疗。图1.NTD-NSAA和TD-NSAA患者的预后情况
TD-NSAA易并发重要脏器功能损伤
且疾病进展风险高
目前对TD-NSAA患者的临床特征知之甚少,我国研究者近期开展了一项回顾性研究,纳入了在中国贫血东部协作组注册的124例TD-NSAA患者,分析了他们的临床和实验室资料4。结果显示,124例TD-NSAA患者的中位年龄为32岁,中位病程为38个月。肝和肾功能障碍(42例,33.9%),病毒性肝炎(29例,23.4%),严重感染(29例,23.4%),糖尿病或糖耐量受损(24例,19.4%),高血压(7例,5.6%),口腔溃疡或疱疹(5例,4.0%)是患者的常见并发症。同时,在评估铁负荷的101名患者中,53名患者(52.5%)发生铁过载,而铁过载是疾病进展的独立危险因素。在随访期间,研究者观察到57例(58%)TD-NSAA患者进展为SAA,中位进展时间为24个月。研究者也对所有患者进行了克隆进化评估,显示共有11例患者(8.9%)出现阵发性睡眠性血红蛋白尿症(PNH),发生的中位时间为12.5个月者。另2例患者分别在26个月和120个月时转化为骨髓增生异常综合征,1例患者在22个月时发展为急性髓系白血病。表1.TD-NSAA患者的基线特征
拓展阅读:
临床专家已普遍认知到铁过载会抑制AA患者的骨髓造血功能,影响预后。近期,中国研究者回顾性分析了武汉儿童医院血液科接受异基因造血干细胞移植的SAA患儿临床资料,旨在探索铁过载对SAA患儿移植疗效的影响5。结果显示,与非铁过载组相比,铁过载组患儿在移植后第1个月Treg细胞数量明显减少(3个/μl vs 11个/μl,P=0.045)。铁过载组移植后CMV血症发生率高于非铁过载组(60.0% vs 40.8%),但差异无统计学意义(P=0.144)。此外,与非铁过载组相比,铁过载组出血性膀胱炎发生率显著升高(32.0% vs 10.2%,P=0.027)。基于此,研究者认为SAA诊断明确后应缩短移植前输血依赖期,控制铁过载,降低移植并发症的发生率,以进一步改善SAA患儿接受移植后的长期生存质量。由于年龄、经济条件及有些医生认为TD-NSAA不严重可以等待,既往临床多给予患者以环孢素A(CsA)为主的治疗。我国开展的一项真实世界研究中,接近90%的TD-NSAA患者接受环孢素单药或环孢素联合雄激素2。然而,环孢素单药治疗TD-NSAA的6个月总缓解率不足20%4,联合雄激素的疗效也仅能在此基础上增加30%6。基于此,已有研究者开始探索ATG联合环孢素的免疫抑制治疗(IST)在TD-NSAA患者中的应用,该方案的短期疗效显示出较大的提升,6个月总缓解率可达75%,然而,IST长期疗效不佳,5年EFS率仅35.9%,说明六成以上患者经历了疾病进展、复发及死亡等事件7。此外,ATG须住院进行,常伴有输注反应、血清病反应,安全性尚待提升,且需要保护性隔离、感染预防等支持治疗,费用较昂贵。图2.IST和HSCT治疗TD-NSAA患者的无事件生存情况
造血干细胞移植(HSCT)是目前公认的治愈AA的治疗手段,在TD-NSAA中的应用疗效也已经得到了证实。一项回顾性研究分析了55例TD-NSAA患者,其中27例接受IST,28例接受同种异体HSCT7。结果显示,以ATG为基础的IST组的5年总生存率(OS)为56.5% ,HSCT组为70.3%,两组之间并未显示出差异。但是,限制HSCT应用于AA的因素较多,包括供体和基础设施短缺、经济负担重以及相关并发症发生率高等等,综合来看,仅极少数患者能选择HSCT作为治疗选择。
TPO-RA联合IST已成当前实践标准
海曲泊帕治疗TD-NSAA初显锋芒
随着临床工作者对TD-NSAA危害的深入认知,2022版AA指南已经明确指出TD-NSAA应尽早按照SAA的治疗策略给予治疗,即对无HLA相合同胞供者和年龄>40岁的患者首选免疫抑制治疗((ATG/ALG+CsA)联合TPO-RA和(或)其他促造血的治疗方案。海曲泊帕是一种新型的口服二代小分子、非肽类TPO-RA,其化学结构与艾曲泊帕、阿伐曲泊帕等同类药物不同。既往研究发现联苯结构可能具有肝毒性,海曲泊帕以杂环羧基取代,降低肝脏毒性;用苯并饱和碳环取代二甲苯,增强亲脂性,提高药效,是化学药品1类新药8。近年来,海曲泊帕治疗TD-NSAA已经累积了坚实的循证,为患者带来了多重获益。2023年ASH大会上报道了一项前瞻性研究,纳入24例接受海曲泊帕联合CsA治疗的TD-NSAA患者,匹配了79例仅接受CsA的历史队列作为比较对象,旨在评估海曲泊帕联合CsA治疗TD-NSAA的疗效9。研究结果显示,在第24周时,海曲泊帕联合CsA组的总体缓解率为74%,而CsA组为16%(优势比[OR]:14.7;p<0.001)。在第48周时,海曲泊帕联合CsA组的完全缓解率为23%,而CsA组仅为2%(OR:13.8;p = 0.029)。在起效速度方面,海曲泊帕组实现初始反应时间为11.6周,显著短于CsA组(风险比:5.0;p<0.0001)。此外,CsA单药组有34%患者转化为SAA,海曲泊帕联合CsA组仅8%(P=0.018)。所有患者中,仅1例患者经历了≥3级的不良反应。综合来看,海曲泊帕与CsA联合治疗提高了 TD-NSAA 患者血液学反应的发生率、速度和强度,并降低了他们转化为SAA的风险。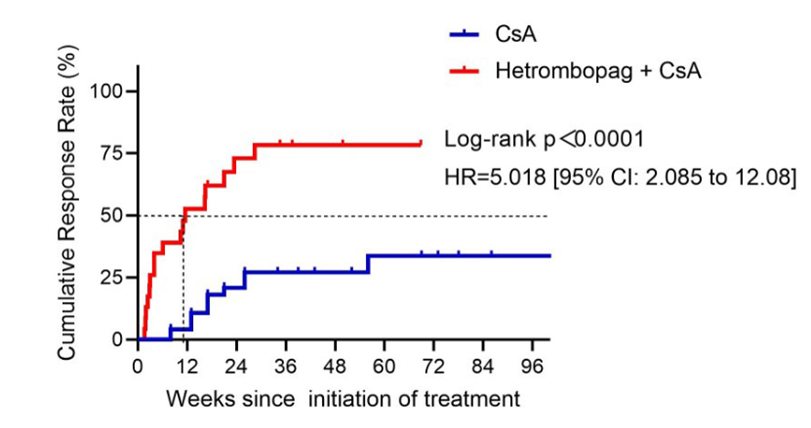 图1.TPO-RA联合CsA和CsA单药自治疗开始后的累积反应率
图1.TPO-RA联合CsA和CsA单药自治疗开始后的累积反应率拓展阅读:
2024年的EHA大会上公布了一项中国前瞻性研究,该研究纳入133例TD-NSAA患者,71例单独接受CsA治疗,62例接受TPO-RA联合CsA治疗,其中23例联合海曲泊帕、22例联合艾曲泊帕、17例联合阿伐曲泊帕,旨在评估TPO-RA联合CsA治疗TD-NSAA的疗效10。TPO-RA+CsA队列和CsA单药治疗队列在3个月、6个月和12个月时的总缓解率分别为51.6% VS 18.3%、72.3% VS 28.1%和79.3% VS 45.2%(P<0.01)。不同TPO-RA在6个月时取得的总缓解率未显示出统计学差异,海曲泊帕组为68.4%,艾曲泊帕组为65.8%,阿伐曲泊帕组为69.7%。此外,TPO-RA联合CsA相较于CsA单药显著降低了疾病进展为SAA的风险(5.7% vs 32.4%,P=0.009),同时还显著提升了2年无事件生存率(54.6% vs 38.7%,P=0.012)。观点评述
从临床工作角度来看,目前医生对TD-NSAA的重视程度不足,未充分认识到该病潜在的严重性以及积极干预的必要性,故指南依从性低,实践中未能完全贯彻最新建议。近年来,TD-NSAA的疾病特点已被研究者逐渐深入了解,该类人群并发症多、铁过载风险及疾病进展风险高,导致生活质量明显下降,同时远期生存不容乐观。以海曲泊帕为代表的TPO-RA联合免疫抑制剂明显提升了TD-NSAA的治疗后的起效速度和血液学缓解率,同时降低疾病进展风险,具有改善患者长期预后的良好潜力。但是,目前TPO-RA在TD-NSAA患者中开展的研究随访时间均较短,仍需在长期随访中评估远期疗效、克隆演变风险等,相信随着未来研究结果的公布,临床对于TPO-RA在该人群中的应用将更加明确,治疗模式也将持续向规范化和精准化发展。 参考文献
参考文献
1. Zhu XF, et al. Acta Haematol. 2019;142(3):162-170.
2. 中华医学会血液学分会红细胞疾病(贫血)学组.中华血液学杂志, 2022, 43(11) : 881-888.
3. Zhang XT, et al Hematology. 2021 Dec;26(1):1025-1030.
4. Zhang Y, et al. Front Immunol. 2023 Jul 11;14:1197982.
5. 晏黎,等. 中华血液学杂志, 2024, 45(6) : 586-590.
6. 宋琳,等. 中华血液学杂志, 2016, 37(11) : 946-951.
7. Shen Y, et al. Ann Med. 2023;55(2):2271475.
8. 张子颖 ,等.中国药学杂志, 2024, 59(15): 1361-1365
9. Yuemin Gong, et al. Blood 2023; 142 (Supplement 1): 1343.
10. Xiaoyu Chen,et al. EHA 2024 Abstract
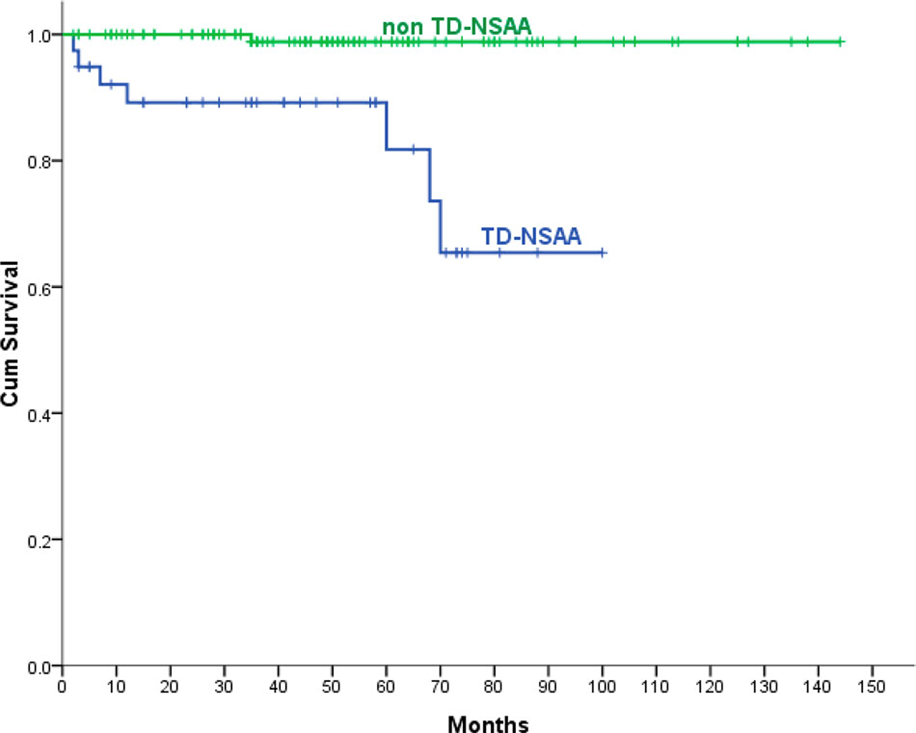
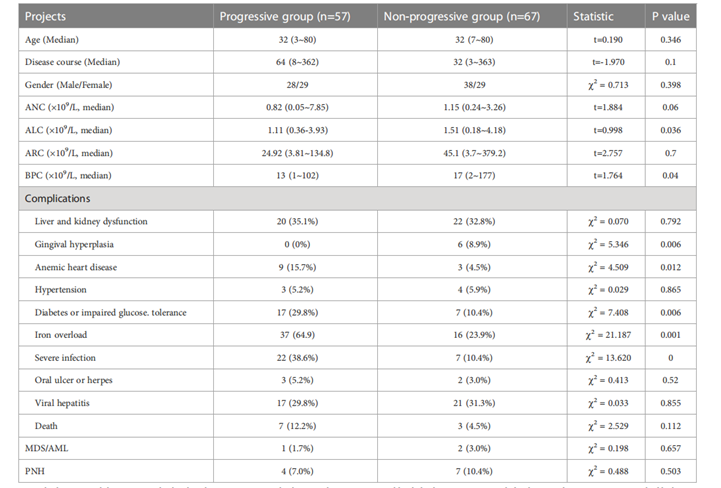
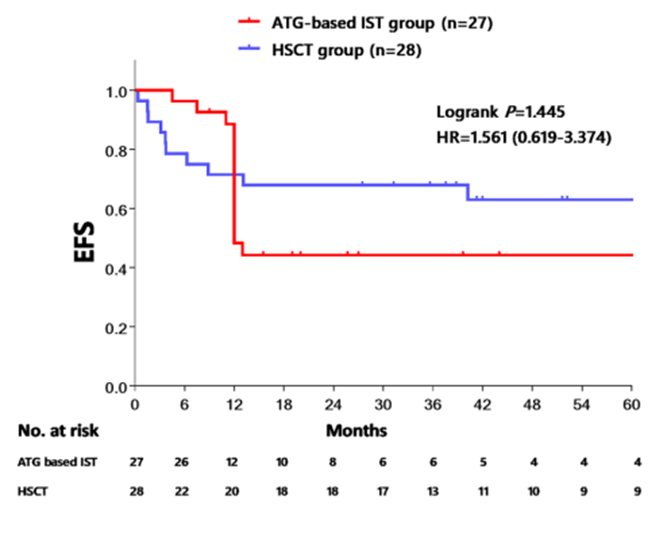
 图1.TPO-RA联合CsA和CsA单药自治疗开始后的累积反应率
图1.TPO-RA联合CsA和CsA单药自治疗开始后的累积反应率 参考文献
参考文献











