TD-NSAA患者生活质量显著降低、预后较差,且面临沉重经济负担
拓展阅读:
关于AA的发病机制,目前认为T细胞异常活化、功能性亢进造成骨髓损伤是原发性获得性AA的主要发病机制。新近研究显示辅助性T细胞亚群Th1/Th2分化偏移、调节性T细胞(Treg)及自然杀伤细胞(NK细胞)调节功能不足、Th17、树突状细胞(DC细胞)以及巨噬细胞等功能异常甚至某些遗传背景都参与了AA发病4。以上发病机制提示AA的治疗可从减少骨髓损伤入手,抑制异常的免疫反应,达到缓解病情的目的。
IST作为AA最常使用的治疗措施,虽然短期疗效可观,但长期疗效并不理想。相关研究发现,AA患者(其中TD-NSAA患者占比49%)接受CsA治疗6个月总体应答率(ORR)达73%,接受抗胸腺细胞球蛋白(ATG)联合CsA治疗6个月ORR达74%3。然而,另一项研究显示TD-NSAA患者接受ATG联合CsA治疗12个月时,ORR降至56.7%6。此外,AA患者接受IST时疾病复发率、感染率均较高(11年复发率45%、10个月感染率38.5%)11,12。上述数据提示,TD-NSAA的治疗仍充满挑战,临床亟需更优治疗方案。
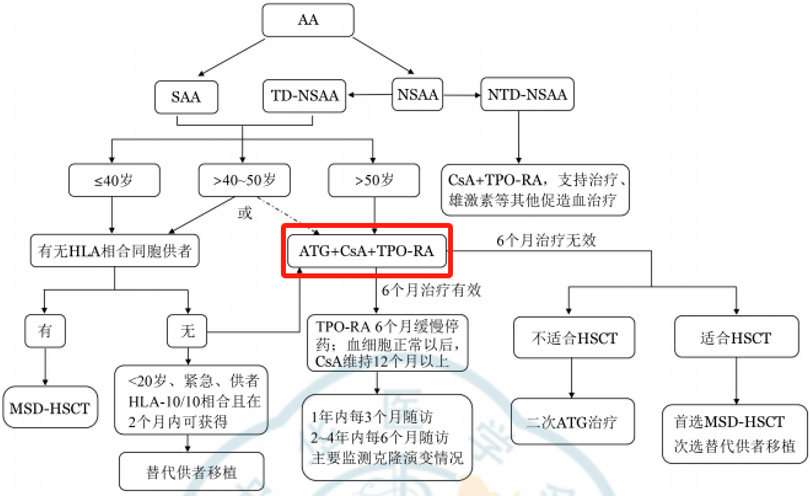
图1. AA治疗路线图
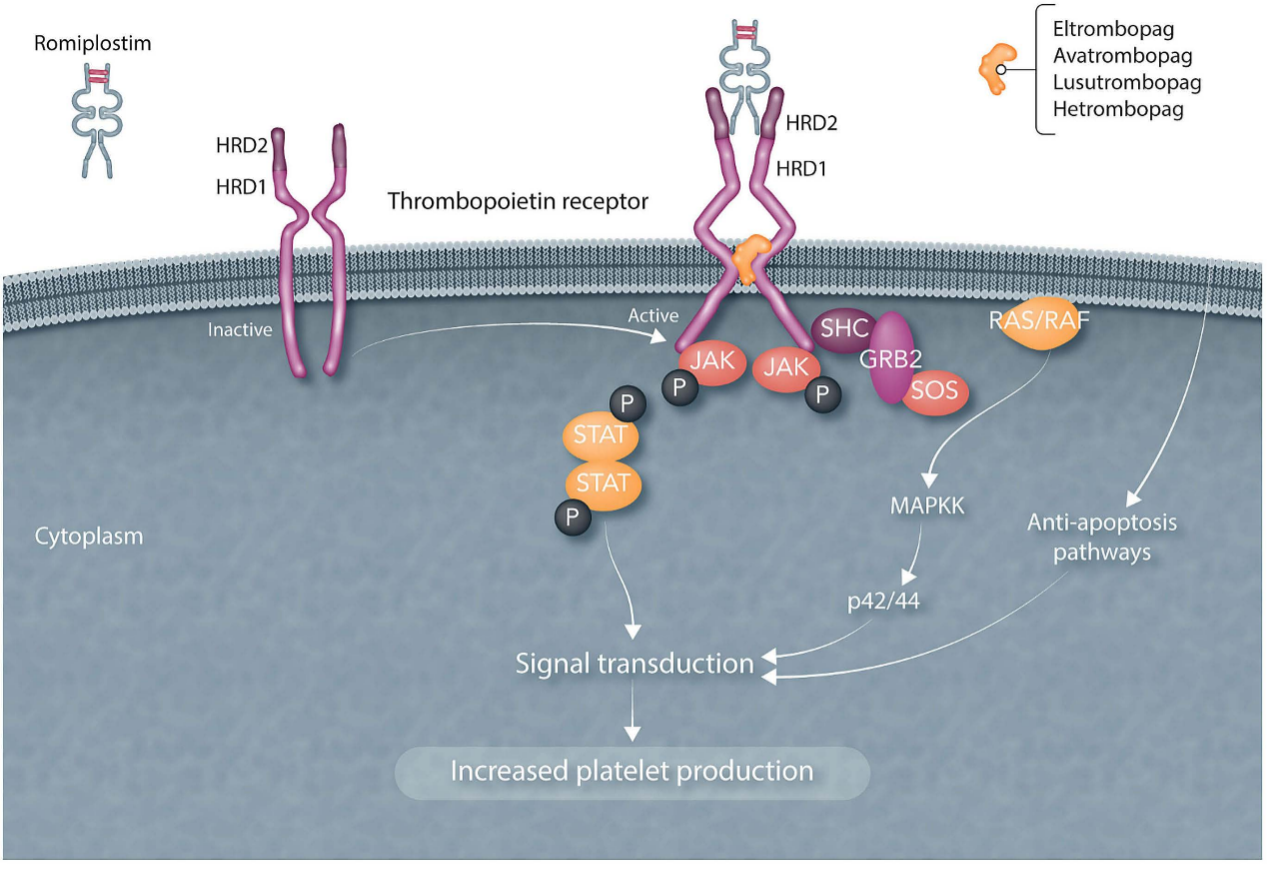
图2. TPO-RA的促造血作用机制
除上述海曲泊帕用于成人患者的研究之外,还有一项探索海曲泊帕用于儿童TD-NSAA患者长期随访结果的研究表明,海曲泊帕用于儿童患者,中、长期疗效较好且可保持稳定(6个月、12个月ORR均为75%)21。
撰文:

责编:

参考文献:
1.Liu T, Pan Y, Ye M, et al. Experience of life quality from patients with aplastic anemia: a descriptive qualitative study. Orphanet J Rare Dis. 2023 Dec 21;18(1):393.
2.Fattizzo B, Gurnari C, Cassanello G, et al. Deciphering treatment patterns in non-severe/moderate aplastic anemia: an international observational study. Leukemia. 2023 Dec;37(12):2479-2485.
3.中华医学会血液学分会红细胞疾病(贫血)学组. 再生障碍性贫血诊断与治疗中国指南(2022年版)[J]. 中华血液学杂志,2022,43(11):881-888.
4.陈芳菲,郭智玮,张立男,等. 52例非重型再生障碍性贫血患者环孢素A治疗前后生活质量的变化研究[J]. 中华血液学杂志,2020,41(10):806-810.
5.Zhang Y, He Y, Wang S, et al. Transfusion-dependent non-severe aplastic anemia: characteristics and outcomes in the clinic. Front Immunol. 2023 Jul 11;14:1197982.
6.Norasetthada L, Wongkhantee S, Chaipokam J, et al. Adult aplastic anemia in Thailand: incidence and treatment outcome from a prospective nationwide population-based study. Ann Hematol. 2021 Oct;100(10):2443-2452.
7.Zhang MX, Wang Q, Wang XQ. Hematopoietic Stem-Cell Transplantation versus Immunosuppressive Therapy in Patients with Adult Acquired Severe Aplastic Anemia: A Cost-Effectiveness Analysis. Int J Gen Med. 2021 Jul 15;14:3529-3537.
8.Young NS, Calado RT, Scheinberg P. Current concepts in the pathophysiology and treatment of aplastic anemia. Blood. 2006 Oct 15;108(8):2509-19.
9.Zhu XF, He HL, Wang SQ, et al. Current Treatment Patterns of Aplastic Anemia in China: A Prospective Cohort Registry Study. Acta Haematol. 2019;142(3):162-170.
10.金朋,施均,李星鑫,等. 再生障碍性贫血患者铁代谢异常及铁过载状况研究[J]. 中华血液学杂志,2013,34(10):877-882.
11.Frickhofen N, Heimpel H, Kaltwasser JP, et al. Antithymocyte globulin with or without cyclosporin A: 11-year follow-up of a randomized trial comparing treatments of aplastic anemia. Blood. 2003 Feb 15;101(4):1236-42.
12.曹红,何秋连,马春蓉,等. 国产抗胸腺/淋巴细胞球蛋白联合环孢素A治疗非重型再生障碍性贫血的临床观察[J]. 成都医学院学报,2012,7(1):121-122.
13.Kuter DJ. Treatment of chemotherapy-induced thrombocytopenia in patients with non-hematologic malignancies. Haematologica. 2022 Jun 1;107(6):1243-1263.
14.中华医学会血液学分会血栓与止血学组. 促血小板生成药物临床应用管理中国专家共识(2023年版)[J]. 中华血液学杂志,2023,44(7):535-542.
15.Syed YY. Hetrombopag: First Approval. Drugs. 2021 Sep;81(13):1581-1585.
16.Vlachodimitropoulou E, Chen YL, Garbowski M, et al. Eltrombopag: a powerful chelator of cellular or extracellular iron(III) alone or combined with a second chelator. Blood. 2017 Oct 26;130(17):1923-1933.
17.EHA 2024. P1925.
18.EHA 2024. PB2049.
19.ASH 2023. Abstrac No 1343.
20.ASH 2023. Abstrac No 5005.












