
期刊:Journal for ImmunoTherapy of Cancer
影响因子:10.9
背景
近年来,随着医疗水平提高,强化化疗、自体干细胞移植以及单抗等治疗手段进一步发展,高危NB的治疗效果也得到了提高,然而,高危患者的长期生存率仍不足50%,也有着不低的复发率,总体预后仍不理想。
双唾液酸神经节苷脂抗原(GD2)是神经外胚层起源的肿瘤细胞表达的一种表面抗原,再正常组织中表达有限,但在许多肿瘤中高表达,NB的GD2表达比例可达到100%,因此可作为NB的特异性治疗靶点,此前已有研究表明,GD2单抗对NB的微小残留病灶有效,并且已有相应药物上市。
基于这种情况,研究人员假设使用GD2Bi武装的活化自体T细胞(ATC)靶向NB及其他GD2高表达的肿瘤可能是一种安全有效的策略。在临床前研究中,GD2BATs可有效杀死GD2高表达肿瘤细胞,增殖并在与GD2高表达肿瘤靶点接触时诱导Th1型细胞因子的释放。通过3+3剂量递增1期研究以及基于剂量3的2期研究,评估GD2BATs治疗GD2高表达恶性肿瘤的可行性。
结果
1. 1/2期研究共纳入15名接受过大量既往治疗的NB患者
2013年11月至2017年12月,共有12名患者参加了1期研究,9名完成了治疗,其中有5例NB患者,3例骨肉瘤(OST)及1例促纤维增生性小圆细胞瘤(DSRCT)患者;另外12名NB患者被纳入2期研究,其中10人接受并完成了治疗。所有1期NB患者均在接受清髓化疗后进行了细胞移植(SCT),所有患者均伴随骨髓受累,其中14例NB患者既往接受过GD2单抗治疗。
2. 经过六次输注,部分患者病情得到控制并有所改善
1期研究遵循标准的 3+3 剂量递增设计,剂量水平为40、80和160×106GD2 BATs/kg/每周输注两次,分8次输注,总计 0.32、0.64 或 1.28×109细胞/kg。低剂量 IL-2(300,000 IU/m2/天)和每两周一次皮下 GM-CSF(250 μg/m2/剂量),在第一次GD2BAT输注前3天开始给药。
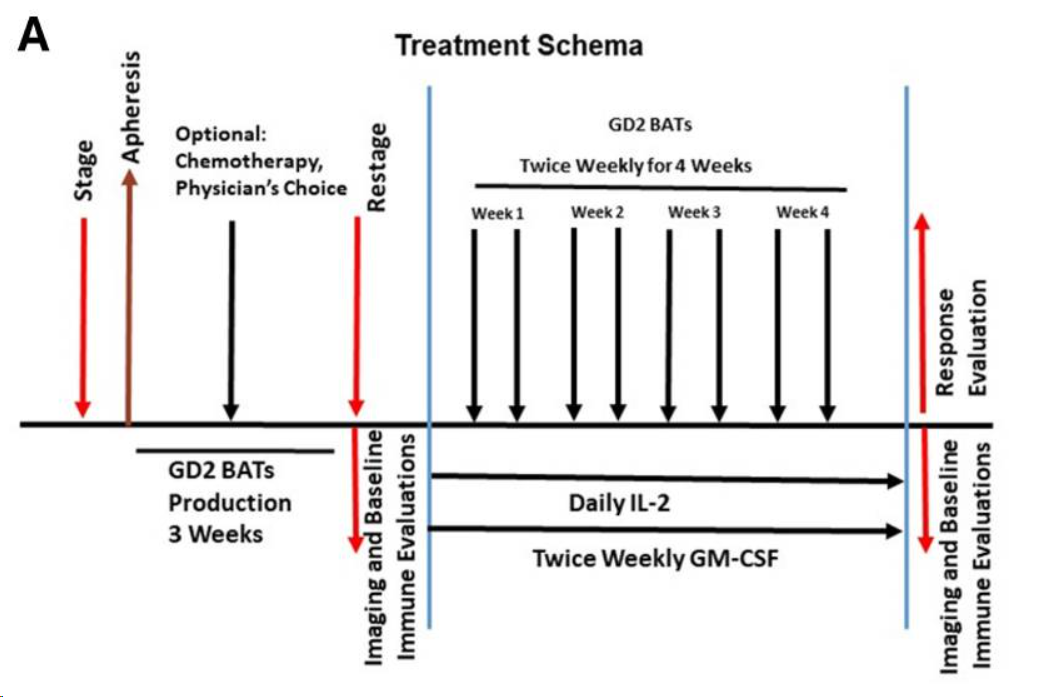
在1期研究阶段,所有患者均未达客观缓解,5例NB患者中3例出现了疾病进展(PD),2例疾病稳定(SD),在治疗结束后,4例NB患者接受了额外治疗。1期组的中位OS为18.0个月。
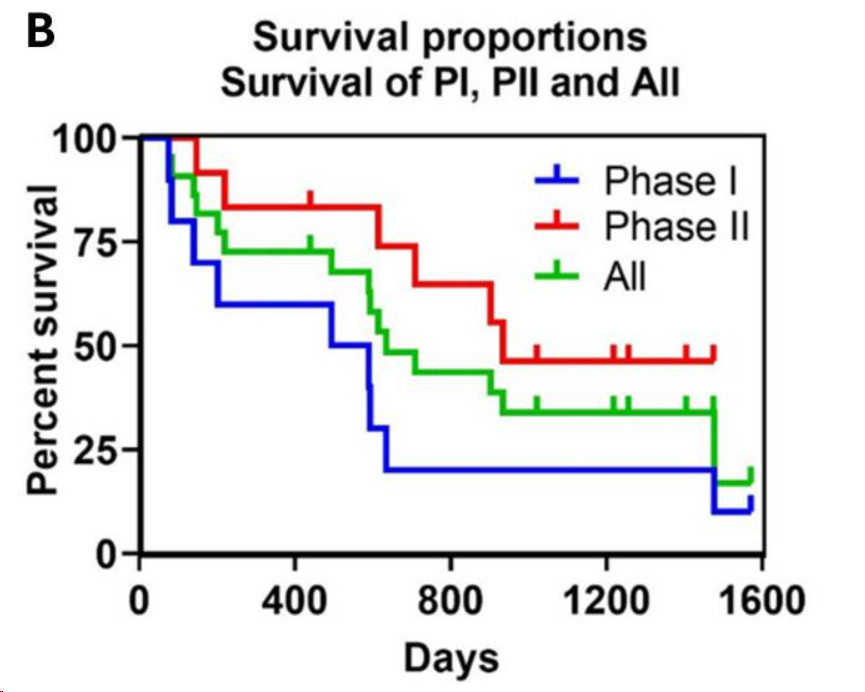
图2. 1/2期患者OS曲线
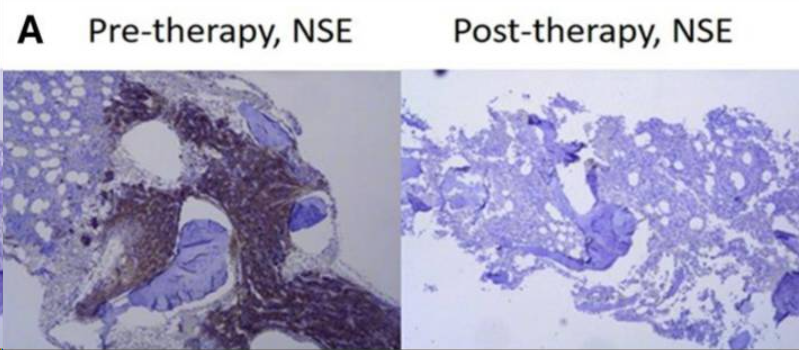
在2期研究阶段,所有NB患者中1名患者达到了部分缓解(PR),5例患者SD,4例患者PD,2期患者的中位OS为31.2个月。这位达到PR的患者患有复发性NB,胸胸腹部软组织受累,在接受治疗后,所有病变均实现PR,在没有额外治疗的情况下,6个月后疾病进展。所有5名SD患者都接受了额外治疗。
3. GD2BAT持久性较高,具有一定细胞毒性且可以激活免疫应答
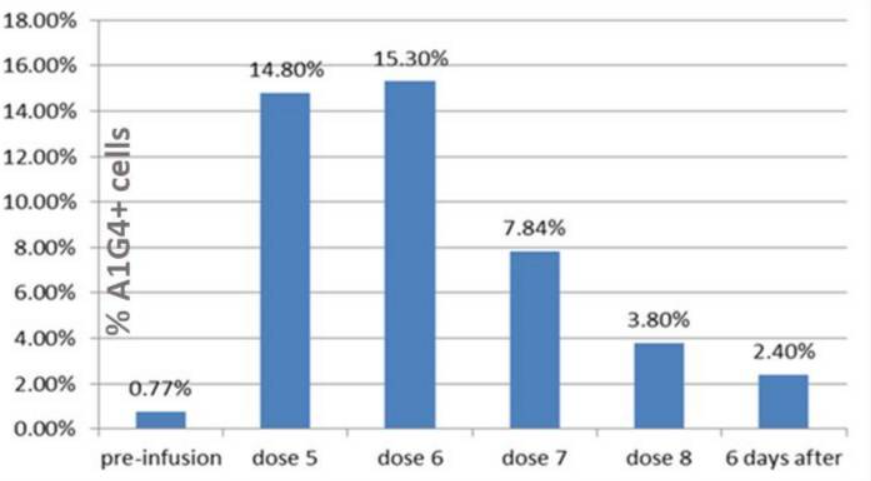
研究人员通过染色对患者PBMC中GD2BAT进行观察,发现GD2BAT数量高于基线,在最后一次输注的六天后,循环中检测到的GD2BAT占PBMC的2.4%。
在治疗1个月后,2期研究中10例NB患者对KCNR(NB细胞系)和MG63(OST,细胞系)细胞系的反应明显增强,而对K562(NK靶向细胞)的反应无统计学意义,1期患者中则没有显示出显著差异。综合来看,治疗后患者对KCNR和MG63的治疗水平显著高于治疗前。NK活性的变化则不明显。
与治疗前相比,治疗后患者体内IL-12、MIP1β以及IL-10均明显升高,而IL-6、TNFα和IP-10则未表现出明显变化。
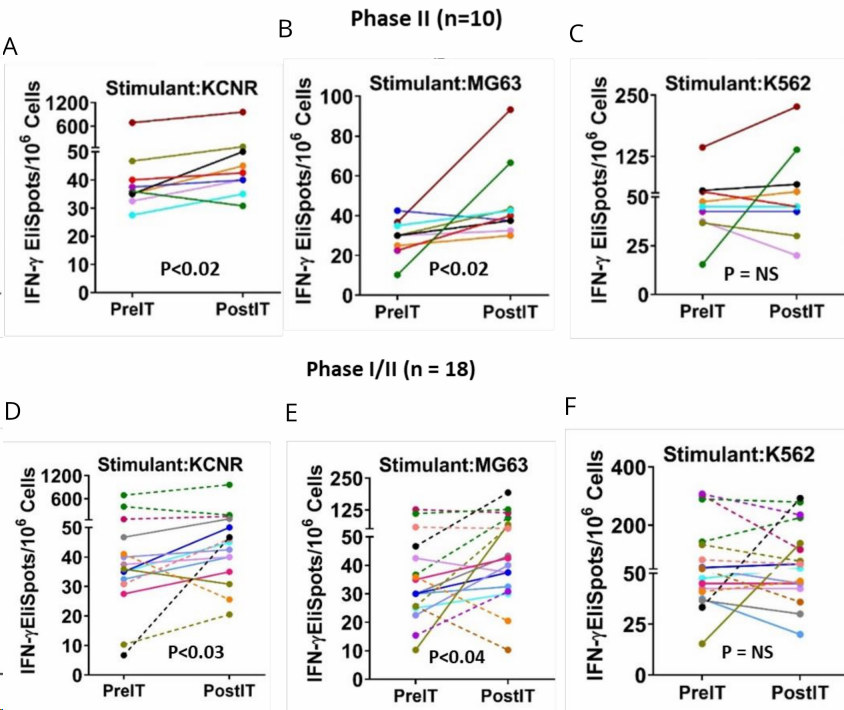
图5. 治疗前后对于肿瘤细胞系反应变化
4. 所有患者均出现轻度CRS,但所有不良反应均在72小时内减退
1期研究中9例患者共接受了72次GD2BAT输注,没有患者因为不良反应而停止治疗。所有患者均出现了轻度CRS,伴有1-3级发热、寒战、头痛、恶心,部分患者出现1-2级低血压。发热、寒战为最常见的2级和3级毒性。2期研究中的患者经历了类似的毒性,没有出现剂量限制性毒性(DLT),并且所有毒性均在72小时内消退至3级以下。
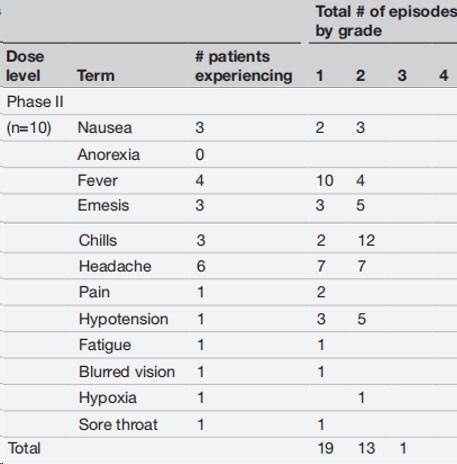
图6. 2期研究中患者不良反应
讨论
尽管已有GD2单抗药物上市,但仍有相当一部分高危NB患者缺乏有效的治疗手段。在一线治疗不成功后,MIBG、激酶抑制剂、GD2抗体等治疗手段在复发或难治性NB中治疗效果同样有限。
目前,已有部分研究人员将目光投向GD2 CAR-T药物,这种基于CAR的疗法与BATs之间的主要区别是,CAR-T疗法涉及病毒基因构建体,而用于武装ATC的BiAb是通过临床级mAb的异位偶联产生的;CAR-T需要遇到目标靶点才能被激活,而BATs在体外扩增时被激活,随后通过与肿瘤结合在体内重新激活;CAR-T是长效细胞,能够在体内持续存扩增,具有肿瘤控制潜力的同时也具有更高的安全性问题,而BAT是寿命有限的凋亡前细胞,扩增有限。
另外,临床试验数据表明,GD2 CAR-T细胞的客观缓解率不佳,然而,意大利的一个小组的研究报告显示,其ORR达到了63%。
从试验数据来看,在儿科门诊输注GD2BAT是可行的,患者耐受性良好,不良反应的风险较低,主要不良反应均在72小时内消退且不超过2级;尽管1期研究中没有患者达到客观缓解,但在部分患者中GD2BAT表现出了一定疗效,并且对于此前失败的化疗方案有反应,表明GD2BAT可能会使肿瘤“敏感”,也使得化疗有效性进一步提高;而在2期研究中,部分患者的病情得到缓解。
参考文献:












