化疗药物相关血小板减少(CIT)是肿瘤治疗过程中常见的血液学毒性之一,可导致抗肿瘤药物剂量降低、治疗延迟甚至终止,甚至可能增加患者出血风险、对患者的生存造成威胁、提高医疗费用。CIT预防和治疗的主流方式为血小板输注,然而这种方式可能增加传染性疾病风险,以及引起患者体内产生抗血小板抗体导致输注无效或免疫反应。因此,促血小板生成因子应运而生。阿伐曲泊帕是新一代血小板生成素受体激动剂(TPO-RA),它结合并活化血小板生成素(TPO)受体,刺激骨髓巨核细胞的增殖和分化,促进血小板生成。随着阿伐曲泊帕在血小板减少患者中应用的不断增加,研究者们逐渐把目光投向了CIT领域。2022年9月,安徽省肿瘤医院的研究人员于期刊Frontiers in Pharmacology上发表了一项研究,旨在探索阿伐曲泊帕单药用于实体瘤伴CIT患者的有效性和安全性,为它的临床应用提供更多的证据。一项多中心、开放式、单臂研究纳入74例实体瘤伴CIT患者,旨在探索阿伐曲泊帕治疗CIT的有效性和安全性。
研究纳入2020年10月至2021年4月于8个中心就诊的18-75岁、实体瘤(妇科肿瘤、胃肠道肿瘤、肺癌、头颈部肿瘤)、末次化疗后出现≥2级血小板减少(血小板计数10×109-75×109/L)的患者,给予其阿伐曲泊帕片剂(每日口服60 mg,持续5-10天)。若需要,患者可接受紧急治疗。停药的标准为:患者血小板计数增加50×109/L或增加至100×109/L。随访持续4周。
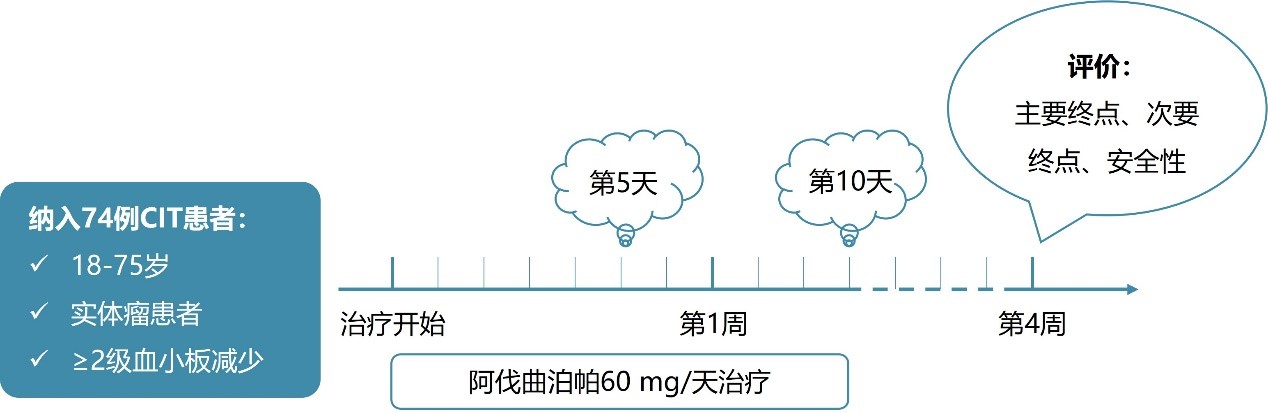
图1. 研究设计
主要终点:治疗开始后,血小板计数≥100×109/L、或增加≥50×109/L、增加≥100%的患者比例。
次要终点:(1)Ⅲ、Ⅳ级血小板减少的持续时间;(2)血小板计数恢复至≥75×109/L和≥100×109/L的时间;(3)最低血小板计数;(4)未接受血小板输注的患者比例;(5)无临床相关出血的患者比例。
研究还记录了治疗期间出现的不良事件(AE)和严重AE(需住院或延长住院时间、致残、误工、威胁生命、致死、致先天性畸形的AE)。
基线特征:患者平均年龄为59.8±11.0岁,男性占比62.2%。各肿瘤占比中,肺癌18.9%,消化道肿瘤56.7%。8.1%患者出现骨转移,40.5%患者出现其他部位转移。13.5%患者伴肝病。正在接受化疗、靶向治疗、免疫治疗的患者占比分别为16.2%、29.7%、13.5%。其他信息见表1。
表1. 患者基线特征
主要终点:4周时,阿伐曲泊帕治疗的累积有效率(符合任一标准)为70.3%。42例(56.8%)患者血小板计数达≥100×109/L,44例(59.5%)患者血小板计数达≥50×109/L,27例(36.5%)患者血小板计数相较基线升高≥100%,见图2: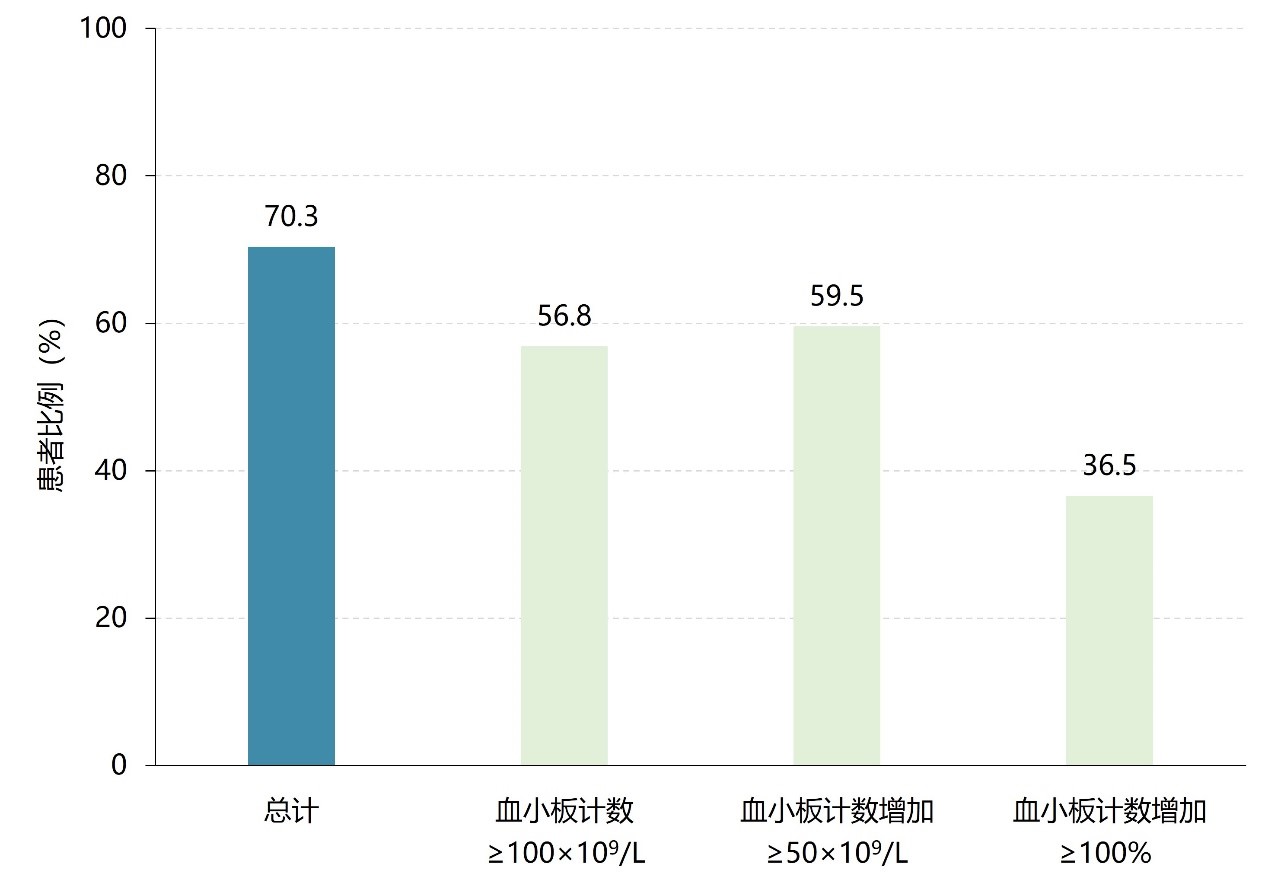
图2. 4周时达到主要终点的患者比例
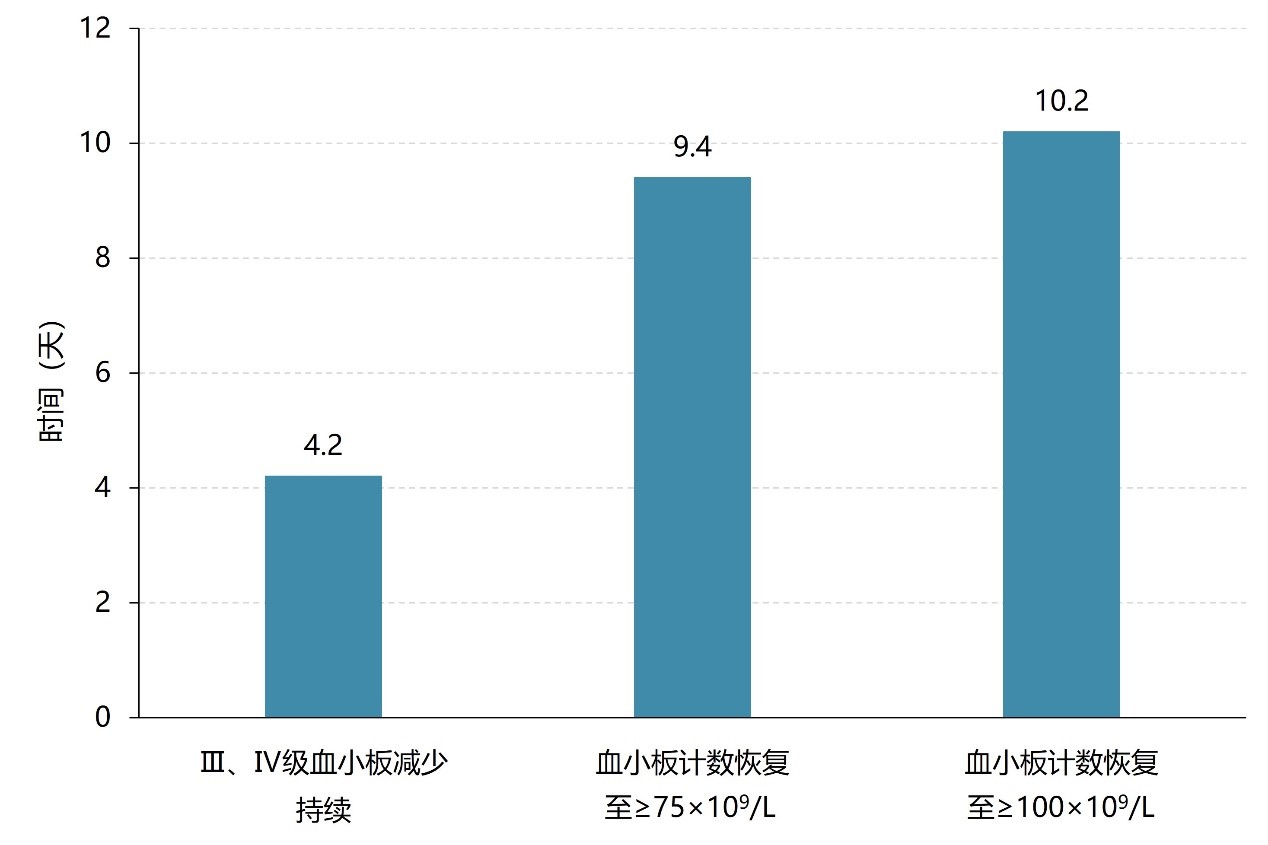
次要终点:Ⅲ、Ⅳ级血小板减少的持续时间为4.2±5.3天。血小板计数恢复至≥75×109/L的时间为9.4±6.6天,恢复至≥100×109/L的时间为10.2±6.4天。见图3:图3. Ⅲ、Ⅳ级血小板减少持续时间和血小板计数恢复时间患者最低血小板计数为(57.9±45.3)×109/L。14例(18.9%)患者需接受血小板输注作为紧急治疗,6例(8.1%)患者发生出血事件,见图4:图4. 接受血小板输注(A)、发生出血(B)的患者比例安全性:研究最常见的AE为恶心(n=6,8.1%)、乏力(n=4,5.4%)和腹痛(n=1,1.4%),未见发热、头痛和外周水肿。
本研究结果显示,阿伐曲泊帕可有效增加实体瘤患者的血小板计数,与既往阿伐曲泊帕用于实体瘤伴重度/难治性CIT患者的研究结果类似,而患者血小板计数恢复的时间略长于另一项使用重组人TPO治疗CIT的研究,可能是因为基线时患者的血小板计数更低。体外研究表明阿伐曲泊帕的结构中无相关毒性基团,无肝脏相关不良事件发生风险,与本研究结果一致。另外,阿伐曲泊帕通过口服给药,避免了针剂相关反应,例如注射部位疼痛和瘀斑。
但是该研究尚有一些局限性:由于未设置平行对照组,以及患者样本量较小因此无法客观探讨阿伐曲泊帕对抗肿瘤治疗的影响。此外,研究未能明确阿伐曲泊帕对各种药物引起CIT的具体影响,也无法确定阿伐曲泊帕的长期疗效和安全性。综上,这项在中国实体瘤CIT患者中进行的研究表明,与基线相比,患者接受阿伐曲泊帕治疗后血小板计数有所增加,且药物安全性、耐受性佳。期待未来能够对阿伐曲泊帕进行更加深入的研究,纳入更多患者、设置平行分组、进行时间更长的随访,甚至可对不同TPO-RA进行头对头研究,以更加客观地评价阿伐曲泊帕治疗抗肿瘤药物相关血小板减少的有效性和安全性,明确其对肿瘤患者预后的影响。参考文献:
Cui Y, He Y, Hu C, Tu C, Huang J, Zhu X, Zang C, Ding K, Zhan B, Zhao Y, Qian L. Avatrombopag for the treatment of thrombocytopenia induced by chemotherapy in patients with solid tumors: A multicenter, open-label, single-arm trial. Front Pharmacol. 2022 Sep 27;13:970978.