各个击破—— 达妥昔单抗β联合化疗有效缓解复发难治性神经母细胞瘤多部位病灶
复发/难治性神经母细胞瘤(R/R NB)的治疗一直是临床上的重大挑战,目前尚无确立的标准治疗方案。已有研究表明,抗GD2单抗免疫疗法对复发或难治性高危神经母细胞瘤具有显著的抗肿瘤活性,且将GD2单抗免疫治疗与化疗相结合,能够显著增强抗肿瘤效果,特别是提高细胞毒性作用。近年来,达妥昔单抗β(dinutuximab beta, DB)作为一种新的GD2单抗,在诱导化疗中应用,已被证实可以有效提升高危神经母细胞瘤患者的反应率和生存率。近期,达妥昔单抗β联合化疗对复发/难治性神经母细胞瘤患者的治疗效果得到了进一步的临床验证,取得了良好的疗效和安全性。2023年2月,波兰Aleksandra Wieczorek教授与德国Holger Lode教授团队在《Frontiers in Oncology》杂志上发表了题为《Dinutuximab beta combined with chemotherapy in patients with relapsed or refractory neuroblastoma》的文章,再次验证了达妥昔单抗β联合化疗对复发/难治性神经母细胞瘤(R/R NB)的有效性与安全性。
这项研究是一项多中心、回顾性、同情用药的临床试验,旨在评估达妥昔单抗β联合化疗在复发/难治性神经母细胞瘤(R/R NB)患者中的疗效与安全性。共有25例患者被纳入研究,其中复发性患者20例(首次复发12例,第2次复发6例,第3次和第5次复发各1例),难治性患者5例。研究者为这些患者制定了一个以达妥昔单抗β为核心的治疗方案,并结合化疗药物TEMIRI(伊立替康和替莫唑胺),评估治疗的综合效果。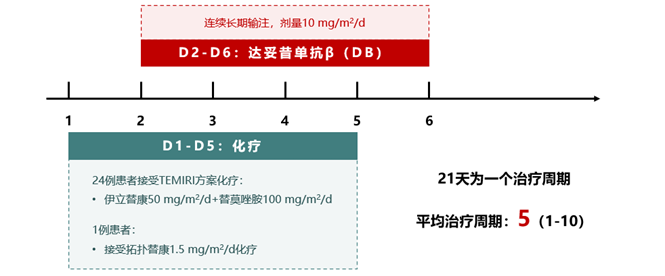
图1. 达妥昔单抗β(DB)联合化疗的研究方案设计本研究中,每个治疗周期使用的达妥昔单抗β总剂量低于说明书推荐的标准剂量,但治疗周期数可根据患者的治疗反应、耐受性和后续治疗计划灵活调整。研究对达妥昔单抗β的治疗周期设定为最多10个周期,通常计划进行5个周期,达到完全缓解(CR)或疾病稳定(SD)的患者,可在此基础上延长治疗。该研究发现,达妥昔单抗β联合TEMIRI化疗方案对复发/难治性神经母细胞瘤患者的疗效显著,总体客观缓解率(ORR)达到64%,完全缓解率(CR)为32%。在亚组分析中,研究人员进一步探讨了不同病灶部位患者的反应情况。数据显示,骨髓转移患者的CR率最高,达到100%;骨转移、软组织病灶以及淋巴结转移的患者,其ORR分别为71%、100%和67%。这表明,达妥昔单抗β联合化疗对多部位病灶的治疗具有显著效果。图2. DB联合化疗治疗R/R NB以及不同病灶部位患者的治疗缓解情况ORR:客观缓解率;CR:完全缓解(率);PR:部分缓解(率);SD:疾病稳定;PD:进展性疾病同时,研究人员通过Kaplan–Meier生存曲线评估了患者的远期生存情况。数据显示,接受治疗的患者在1年内的总生存率(OS)和无进展生存率(PFS)分别为47%和48%;3年时OS和PFS分别为35%和36%。这些数据表明,达妥昔单抗β联合化疗可以显著延长复发/难治性神经母细胞瘤患者的生存期。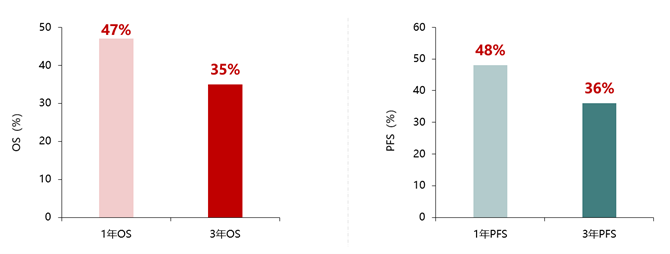
图3. DB联合化疗治疗R/R NB的OS和PFS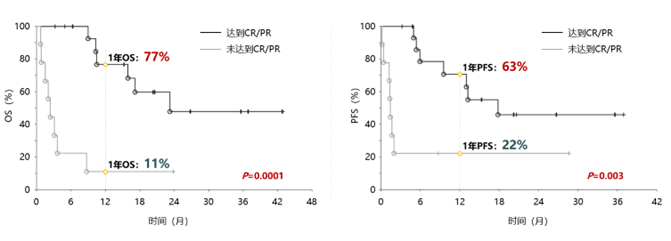
图4. DB联合化疗治疗后达到或未达到CR/PR的R/R NB患者的OS和PFS通过比较不同反应的患者,研究还发现,达到完全缓解(CR)或部分缓解(PR)的患者1年OS和PFS显著高于未达到CR或PR的患者(P<0.05)。
安全性分析
在安全性方面,研究团队关注了治疗过程中可能发生的不良反应。研究中唯一观察到的4级不良反应是血液系统的毒性,此外,3级毛细血管渗漏综合征和过敏反应的发生率均为16%。过敏反应常表现为皮疹或支气管痉挛,可以通过支持性治疗进行控制。整体来看,达妥昔单抗β联合化疗治疗的耐受性良好,大部分患者的副作用是可控的,且很少需要调整或减少药物剂量。本研究表明,达妥昔单抗β联合化疗治疗复发/难治性神经母细胞瘤(R/R NB)的疗效显著,总体客观缓解率为64%,完全缓解率为32%。研究结果表明,达妥昔单抗β不仅能有效缓解多部位病灶,还能够显著延长患者的生存期,且该疗法具有良好的耐受性。此研究为复发/难治性神经母细胞瘤的治疗提供了有力的证据,预示着达妥昔单抗β联合化疗可能成为一种具有广泛应用前景的治疗选择。复发/难治性神经母细胞瘤的治疗仍面临巨大挑战,尤其是对于多部位转移的患者。当前,尽管化疗、免疫疗法和靶向治疗等多种治疗手段已被提出,但仍缺乏一种统一的标准治疗方案。达妥昔单抗β作为一种靶向GD2的单抗,其与化疗的联合应用已显示出强大的协同效应。随着研究的深入,未来这一治疗方案有望成为复发/难治性神经母细胞瘤患者的一种标准治疗方案,为更多患者带来生存希望。
参考文献:
1.Troschke-Meurer S, Zumpe M, Meißner L, et al. Chemotherapeutics Used for High-Risk Neuroblastoma Therapy Improve the Efficacy of Anti-GD2 Antibody Dinutuximab Beta in Preclinical Spheroid Models. Cancers (Basel). 2023;15(3):904.
2.Furman WL, Federico SM, McCarville MB, et al. A Phase II Trial of Hu14.18K322A in Combination with Induction Chemotherapy in Children with Newly Diagnosed High-Risk Neuroblastoma. Clin Cancer Res. 2019;25(21):6320-6328.3.Olgun N, Cecen E, Ince D, et al. Dinutuximab beta plus conventional chemotherapy for relapsed/refractory high-risk neuroblastoma: A single-center experience. Front Oncol. 2022;12:1041443.4.Wieczorek A, Zaniewska-Tekieli A, Ehlert K, et al. Dinutuximab beta combined with chemotherapy in patients with relapsed or refractory neuroblastoma. Front Oncol. 2023;13:1082771.5.袁晓军. 双唾液酸神经节苷脂单克隆抗体治疗儿童高危和复发/难治性神经母细胞瘤研究进展[J]. 世界临床药物, 2022, 43(08):967-974. 作者:歆语健康

















