导 语
ASCO(美国临床肿瘤学会)是世界上最大的也是最具影响力的肿瘤组织,它是一个动态的组织,不仅推进着前沿的研究,提供优秀的教育机会,并定义标准的临床护理实践,也影响着公共政策。
今年ASCO发布的有关儿童肿瘤领域的最新研究成果可谓硕果满枝,今天精选了两篇有关儿童神经系统(包括中枢和外周)肿瘤的前沿成果报告如下。
II 期FIREFLY-1(PNOC026)研究中pan- RAF 抑制剂Tovorafenib在儿童低级别胶质瘤组中的临床活性
● 评估Tovorafenib 单药治疗BRAF突变的pLGG患 儿的有效性和安全性。
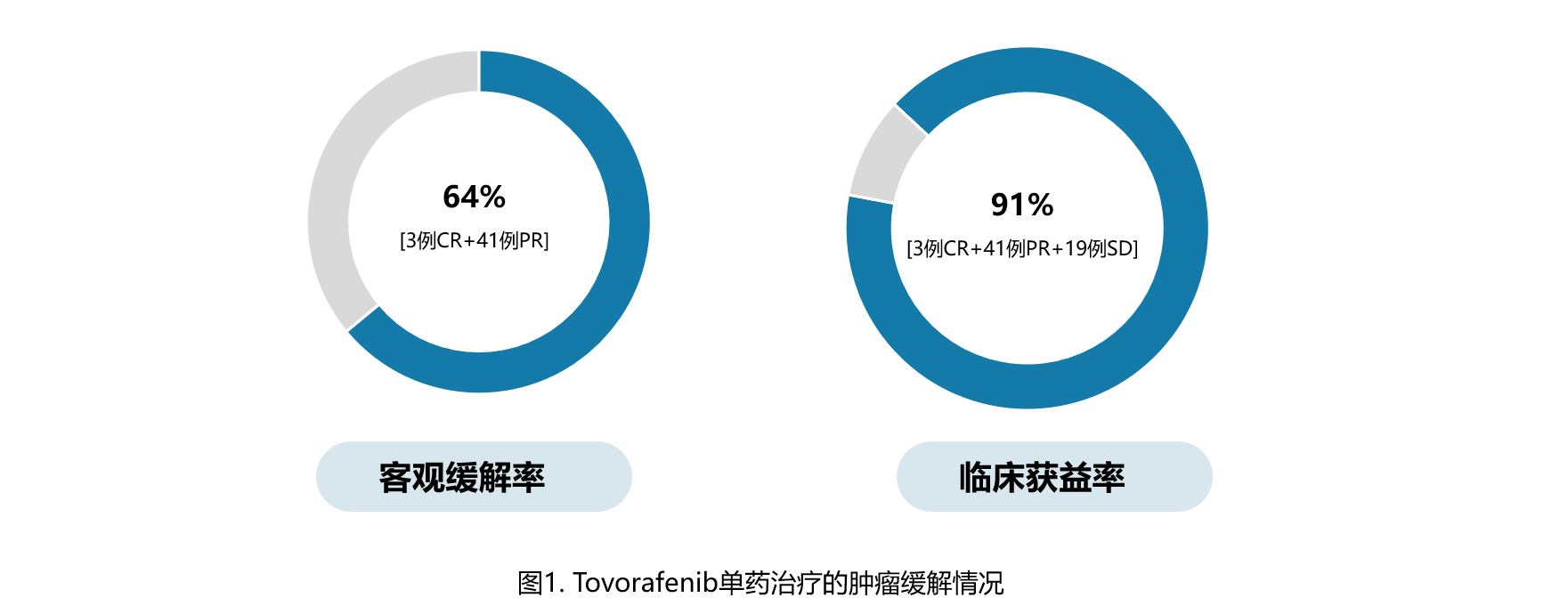
安全性:
● 常见不良事件(TRAE) :毛发颜色改变 (75%)、肌酸磷酸激酶升高 (64%)、贫血(46%)、疲乏 (42%) 和斑丘疹 (42%)。
● TRAE对治疗进程的影响:16例(21%)患者因TRAE调整Tovorafenib剂量,2例(3%)患者因TRAE停药。
● Tovorafenib的耐受性良好,在BRAF 改变的复发/进展性 pLGG 儿童和少年中显示出显著的抗肿瘤活性。
总
结
与
讨
论
迄今为止,根据FIREFLY-1试验所公布的Tovorafenib 单药治疗 BRAF突变的pLGG患 儿的有效性和安全性, Tovorafenib有望为复发性或进展性 pLGG 患者带来更多治疗选择。
一项评估FCN-159 在1型神经纤维瘤病患儿中的安全性和疗效的多中心、开放标签、单组1/2期研究
● 丛状神经纤维瘤(PN) 见于20-50%的 1型神经纤维瘤病(NF1)患者(pts) ,可引起严重并发症。
● Selumetinib在美国和欧盟获批用于 NF1 相关 PN 儿童患者,但在中国的治疗选择仍然有限。
● FCN-159是 MEK1/2 的高效选择性抗致瘤抑制剂,可能对 NF1 相关 PN 有效。
① 确定剂量递增阶段的剂量限制性毒性(DLT)和推荐II期试验剂量(RP2D)。
② 评估FCN-159在 NF1 相关 PN 儿童患者中的有效性和安全性。
剂量限制性毒性(DLT):
● 截至数据截止日期(2022年11月21日),入组了65例患者,I期19例,II期45例。在I期研究中评价了4 mg/m2(10例患者)和5 mg/m2(9例患者)的剂量,未观察到DLT。
推荐II期试验剂量(RP2D):
● 5 mg/m2队列中的儿童患者达到的暴露量与8mg成人队列相似。在不同BSA范围下,群体PK模型的AUC值也与8 mg 成人相似。因此,将RP2D确定为5 mg/m2。
有效性:
● 在19例患者中,8例 (42%) 患者达到PR,11例 (57.8%)达到SD,无患者发生疾病进展。
安全性:
● 常见TEAE(≥20%)为口腔溃疡(43.1%)、窦性心律不齐(36.9%)、上呼吸道感染(35.4%)、毛囊炎(21.5%)、甲沟炎(21.5%)和血肌酸磷酸激酶升高(20%)。
● 5例患者(7.7%)发生≥3级的治疗相关AE(TRAE)未观察到≥4级TRAE。
● 2例患者(3.1%)报告了治疗相关严重不良事件(各1例横纹肌溶解和痤疮样皮炎)。
● 未报告导致剂量降低或死亡的TEAE。
● 总体而言,FCN-159在NF1 相关PN 儿童受试者中耐受良好,并表现出良好的抗肿瘤活性。
总
结
与
讨
论
FCN-159作为一种 MEK1/2 的高效选择性抗致瘤抑制剂,对 NF1 相关 PN 患儿的治疗中展现了其有效性,并且耐受性良好,给儿童NF1 相关 PN的治疗开辟了一条新的治疗路径 。
长期疗效和安全性的结果仍在继续随访,值得持续关注进一步的最新结果。
参考文献:
1.Clinical activity of pan-RAF inhibitor tovorafenib in the registrational pediatric low-grade glioma arm of the phase 2 FIREFLY-1 (PNOC026) study. 2023 by American Society of Clinical Oncology.
2. A multicenter, open-label, single-arm phase 1/2 study to evaluate the safety and efficacy of FCN-159 in pediatric participants with neurofibromatosis type 1. 2023 by American Society of Clinical Oncology.












