导语
司妥昔单抗是一种人-鼠嵌合单克隆抗体(mAb),可阻断白细胞介素-6(IL-6)与IL-6受体相结合,从而阻断下游信号通路,其中IL-6则参与了 B 细胞淋巴恶性肿瘤和多发性骨髓瘤的发病机制。自2014年4月在美国首次获批以来,司妥昔单抗已在全球40多个国家和地区获得批准用于治疗特发性多中心型Castleman病(iMCD)患者,为患者提供了全新的治疗选择。该I期研究主要观察了随给药剂量增加患者是否耐受或是否会出现副作用,并收集司妥昔单抗有关药效学、药动学及有效性的早期数据。

研究设计
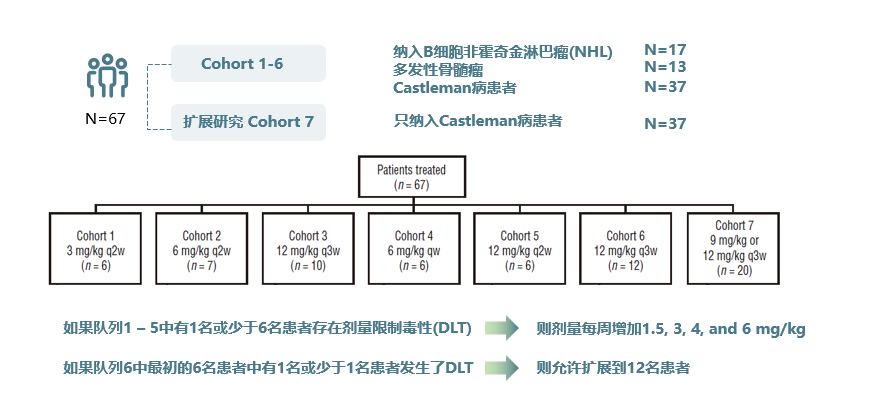
图1. 研究设计
研究结果
除了3 – 4级中性粒细胞减少(21%)和3级高血压(9%)外,大多数不良事件是低度的。NHL、多发性骨髓瘤和Castleman病患者的感染事件率分别为5.2%,1.8%和1.9%。44例(66%)患者在治疗期间至少有一次感染,大多数是低级别感染。与司妥昔单抗无关的最常见感染为上呼吸道感染(URTI;39%)、尿路感染(16%)、鼻窦炎(12%)、蜂窝组织炎(9%)、鼻咽炎(7%)和耳部感染(6%)。
与司妥昔单抗相关的最常报告的不良事件是是血小板减少(25%),中性粒细胞减少(19%),高甘油三酯血症(19%),白细胞减少症(18%),高胆固醇血症(15%),和贫血(10%)。除了中性粒细胞减少和血小板减少(n = 1)外,这些事件均未导致剂量延迟或停药(图2B)。
研究发现队列1 – 6中均未观察到剂量限制毒性(DLT),且1小时静脉滴注与2小时静脉滴注司妥昔单抗的安全性相似;因此,未来所有患者均可以采用1小时滴注,并允许研究中的患者切换至1小时滴注。
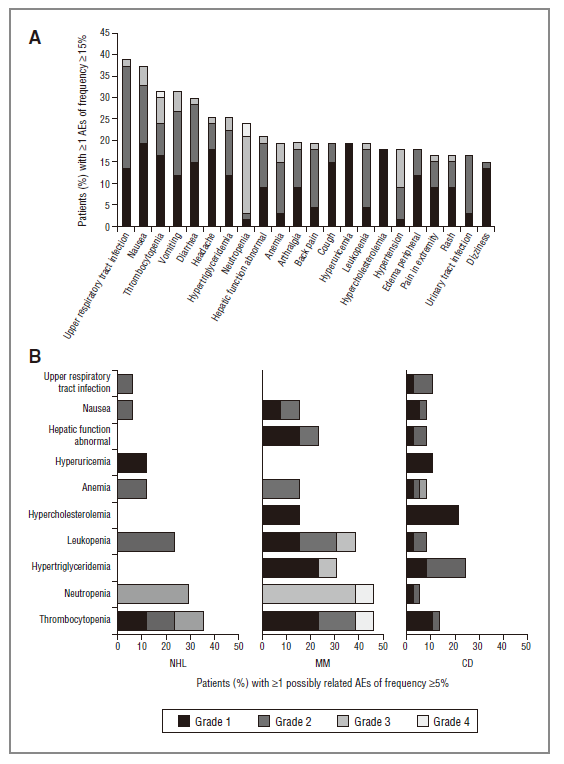
图2. (A)不良事件发生率高于15%的患者比例(%)
(B) NHL、多发性骨髓瘤或Castleman病治疗患者出现≥1个可能与司妥昔单抗相关的不良事件发生率≥5%的患者比例(%)
C反应蛋白(CRP)抑制在用药剂量每3周12mg /kg时最明显。司妥昔单抗的平均终末相半衰期为17.73 ~ 20.64天(表1)。37例Castleman病患者中有32例(86%)获得1个或多个CBR改善;36例Castleman病患者中有12例获得病理学缓解[完全缓解(CR),n=1;部分反应(PR), n=11];在4例对NHL或多发性骨髓瘤有应答的患者中,每3周给予12mg /kg的药物,可以观察到持久应答。
CBR,临床获益反应 (CBR由血红蛋白、疲劳、厌食、发热/盗汗、体重、最大淋巴结大小组成)
药动学( PK) 和药效学( PD)

对于队列1 - 6,研究发现司妥昔单抗的血清浓度呈双指数下降,第一次给药后的平均终末相半衰期为17.73 ~ 20.64天,平均清除率为4.03 ~ 4.59 mL/day/kg。第一次给药和重复给药后,观察到最大浓度(Cmax)和血清浓度-时间曲线下面积(AUC0-t)近似于剂量成比例增加。重复给药后与第一次给药后的终末半衰期一致,表明药代动力学中该指标不受时间变化而变化。当比较NHL、多发性骨髓瘤或Castleman病患者时,未观察到明显的药代动力学差异。
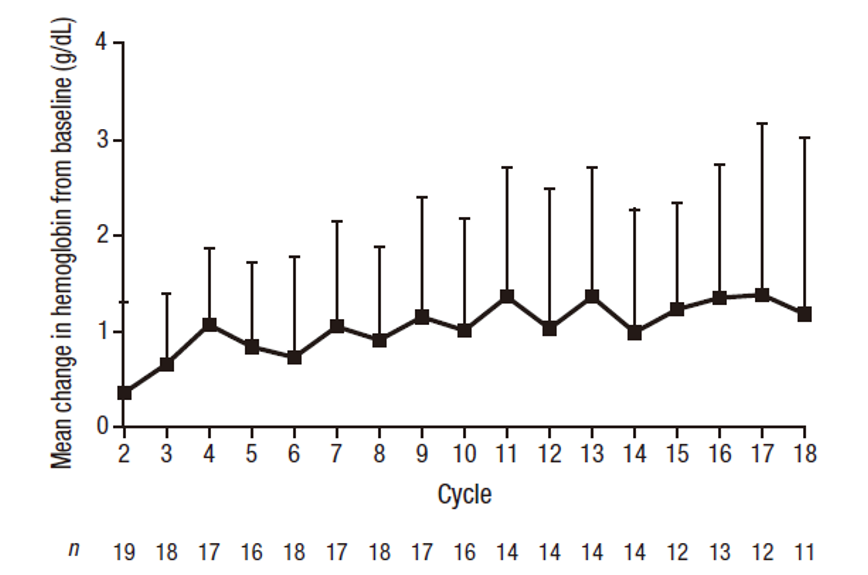
图3. 在队列7中接受治疗的Castleman病患者血红蛋白浓度随时间的平均变化(+ 标准差)
研究结论
在这项I期研究中,67名接受治疗的B细胞NHL、MM或Castleman病患者中,司妥昔单抗的多重给药方案在所有3种疾病类型中均具有良好的耐受性,且没有观察到DLTs。研究者认为与司妥昔单抗有关的最常见的不良事件是血小板减少、中性粒细胞减少、高甘油三酯血症、白细胞减少、高胆固醇血症和贫血,且上述实验室相关的不良事件都是短暂的,可逆的。司妥昔单抗的临床活性在高剂量时最明显,建议给予每3周12mg /kg的剂量。
同时有研究表明IL-6在CD、MM等多种疾病发病或治疗过程中扮演着重要角色,近几年来针对IL-6单抗——司妥昔单抗,有了更为充分的文献报道和循证支持,该药物逐渐成为castleman病等多个疾病领域的学术界关注话题;此类对于适用人群的探索,未来有望让更多患者受益。
参考文献
1. Kurzrock R,et al. Clin Cancer Res. 2013 Jul 1;19(13):3659-70.
END
如需文献全文,请在下方留言并提供您的邮箱












