ASCO 2022速递(二)| 长期安全性扩展研究的事后分析:接受标签给药的iMCD患者对司妥昔单抗的反应
导语
近年来,研究发现iMCD淋巴结肿大和相应病理变化可能是对细胞因子风暴中白细胞介素-6(IL-6)升高产生的反应性变化1-2。以抗IL-6单克隆抗体司妥昔单抗为首的治疗药物的横空出世,填补了iMCD治疗领域的空白。2022年6月3日-7日,美国临床肿瘤学会(ASCO)年会在芝加哥召开,该会议展示了各领域药物的临床最新研究,讨论了当前阶段最先进的治疗方法。上期我们分享了iMCD领域最前沿的信息,本期我们将继续分享由Jean-Francois Rossi教授团队报告的“长期安全性扩展研究的事后分析:接受标签给药的iMCD患者对司妥昔单抗的反应”3。

研究背景
司妥昔单抗是唯一获得美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)批准的iMCD治疗药物。一项为期6年的长期安全性扩展研究,纳入1期或2期试验中对治疗有反应或病情稳定的患者,证实了司妥昔单抗的长期疗效和安全性。然而药物使用剂量尚无统一标准,临床医生可以结合对病情的判断调整使用剂量;在这些扩展研究的60例iMCD患者中,有33例保持每3周给药11 mg/kg,本研究对这些患者进行了事后分析,旨在评估长期标签给药的安全性和有效性。

研究设计
结果
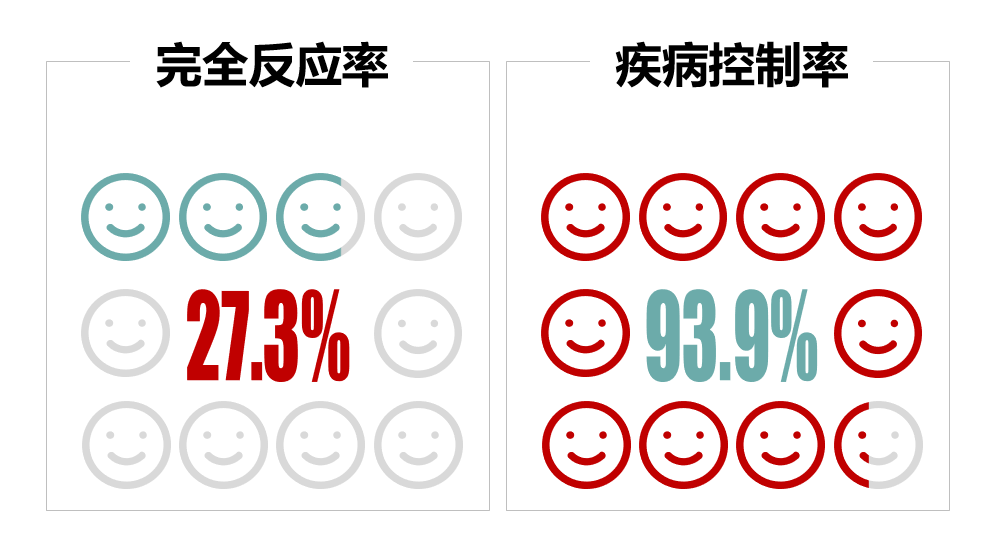
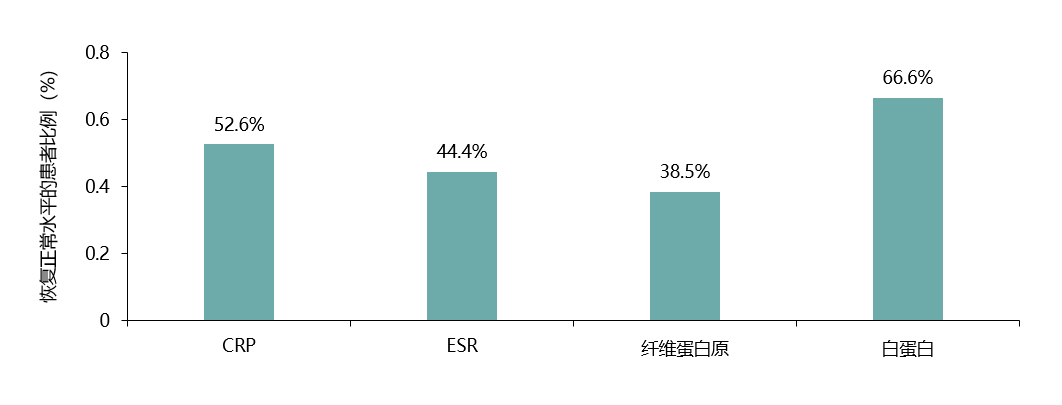
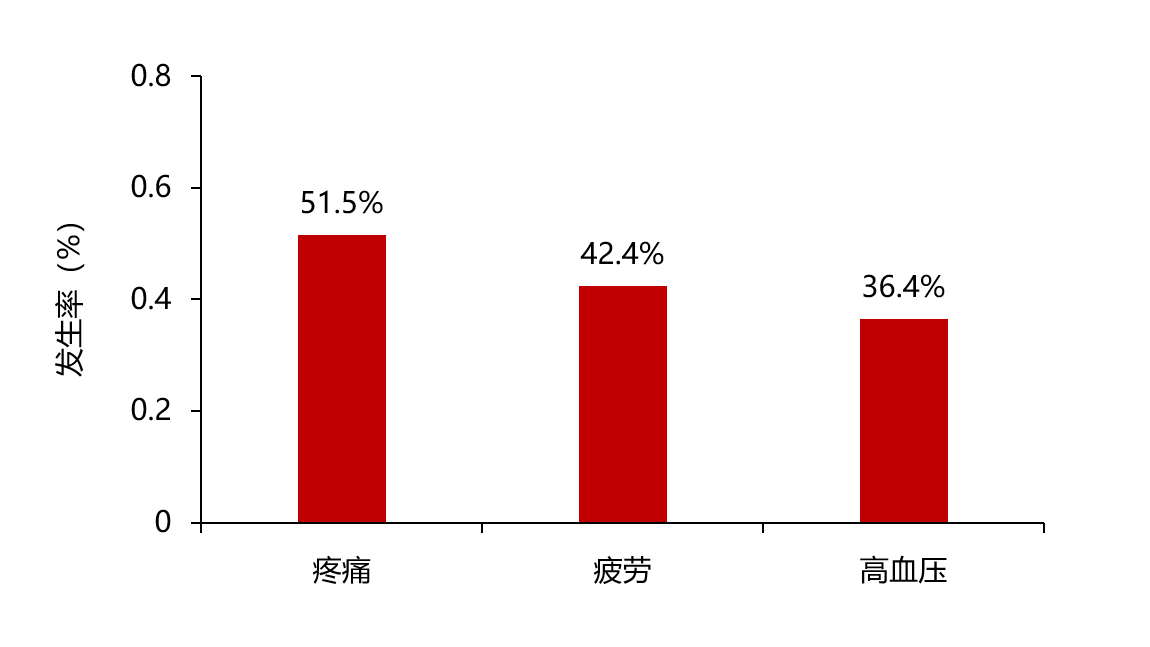
结论
尽管抗IL-6靶向药物司妥昔单抗已经获得FDA和EMA批准用于iMCD治疗,然而真实世界中的使用率并不高,司妥昔单抗的研究与应用仍然任重道远。Jean-Francois Rossi教授团队的研究进一步分析了以往研究中接受长期标签给药的iMCD对司妥昔单抗的反应,再次证实了司妥昔单抗对于iMCD患者的有效性和安全性,给临床用药提供了更多的支持。
END
如需文献全文,请在下方留言并提供您的邮箱
作者:歆语健康
友情链接 歆语健康—上海歆语网络科技有限公司
互联网药品信息服务资格证书编号:(沪)-非经营性-2022-0087












